Bildgebende Verfahren in der Neurologie: Magnetresonanztomographie
Leiter der AG Neuroimaging:
Prof. Dr. med. J. Kassubek
Mitarbeiter der AG:
Prof. Dr. rer. nat. H.-P. Müller
Der wissenschaftliche Fokus
Der wissenschaftliche Fokus der AG Computational Neuroimaging ist die multiparametrische strukturelle, mikrostrukturelle und funktionelle MRT-Bildgebung des Gehirns zur Entwicklung von Neuroimaging-Markern neurodegenerativer Erkrankungen. Der Schwerpunkt der Arbeitsgruppe liegt hier auf der Weiterentwicklung der in der Arbeitsgruppe entwickelten Pre- und Postprocessing-Protokolle für multizentrisch akquirierte Datenkollektive (Plattform TIFT – Tensor Imaging and Fiber Tracking) und der Weiterentwicklung des translationalen Ansatzes im Tiermodell bei der mikrostrukturellen und funktionellen Kleintier-Gehirn-MRT.
Parkinsonsyndrome
In einer longitudinalen Multicenter-Initiative mit Fokus auf die demenzielle Entwicklung bei M. Parkinson (LANDSCAPE-Studie) wurden über 600 strukturelle MR Datensätze aus 6 nationalen Zentren (Dresden, Frankfurt, Kiel, Marburg, Tübingen, Ulm) unter Federführung von Ulm ausgewertet. Longitudinal werden strukturelle Konnektivitätsanalysen in Abhängigkeit vom kognitiven Status durchgeführt. Strukturell zeigen sich bereits bei nicht-dementen Parkinsonpatienten Veränderungen, die sich mittels DTI insbesondere in subkortikalen Strukturen nachweisen lassen, aber noch kompensiert werden können. Als Korrelat kognitiver Beeinträchtigung zeigen sich primär in Gedächtnisassozierten Arealen im Temporallappen und im Hippocampus mikrostrukturelle Schädigungsmuster (Gorges et al., Ther Adv Neurol Disord 2019).
Einer longitudinal angelegten Analyse morphologischer Veränderungen mittels Atlas-basierter Volumetrie (in Zusammenarbeit mit Prof. Dr. H.-J. Huppertz, Schweizerisches Epilepsiezentrum Zürich) und Analysen der kortikalen Dicke konnten longitudinale Volumenverluste bereits bei nicht-dementen Patienten sowie eine regionale Ausdünnung der Hirnrinde nachgewiesen werden (Gorges et al., Hum Brain Mapp 2020).
Für die Multisystematrophie (MSA) ist eine weiter führende Analyse der advanced MRI-Datensätze (DTI) der Daten der PROMESA-Studie (Safety and efficacy of epigallocatechin gallate in multiple system atrophy; Levin et al., Lancet Neurol 2019) durch die AG NeuroImaging der Universität Ulm als Analysezentrum derzeit in Planung.
Motoneuronerkrankungen
Über die Aktivitäten der internationalen NeuroImaging Society in Amyotrophic Lateral Sclerosis (NiSALS), die in Oxford, UK, das jährliche Arbeitsgruppentreffen abhielt, hinaus erfolgte die Validierung mono- und multizentrischer Ergebnisse zu mikrostrukturellen Veränderungen bei der ALS mittels Diffusionstensorbildgebung (DTI) im Rahmen eines multizentrischen Ansatzes: Basierend auf der Expertise der AG NeuroImaging der Universität Ulm als Analysezentrum wurden weitere Untersuchungen zu longitudinalen DTI-basierten mikrostrukturellen Veränderungen bei der ALS in Zusammenarbeit mit Prof. Kalra, University of Alberta, Kanada und den Bildgebungszentren des Canadian ALS Neuroimaging Consortium (CALSNIC) finalisiert (Kalra et al., 2020).
Morbus Huntington
Im Rahmen des Europäischen M. Huntington-Netzwerkes, in das die Neurologische Klinik Ulm auch im Bildgebungsbereich eng involviert ist, wurde im Zusammenhang von internationalen MRT-basierten Studien zum M. Huntington einschließlich präsymptomatischer Genträger im Querschnitts- und Longitudinal-Design eine Initiative gestartet zur MRT-basierten Analyse struktureller Veränderungen in Relation zu funktioneller und mikrostruktureller Konnektivität mit dem Ziel der Etablierung der multiparametrischen MRT als biologischer Marker für klinische Studien. Die Methode der Atlas-basierten Volumetrie wurde bei M. Huntington erfolgreich angewendet zur Untersuchung von longitudinalen Veränderungen des Striatums als Studien-Read out (mit erstmaliger Etablierung entsprechender Effektgrößen) (Müller et al., Parkinsonism Relat Disord, 2019).
Frontotemporale Lobärdegeneration
Die AG Neuroimagingist ein Koordinationszentrum hinsichtlich der MRT-Akquisition und Datenauswertung des Netzwerks für fronto-temporale Lobärdegenerationen, gemeinsam mit Prof. Dr. M. L. Schroeter (Leipzig).
MRT-Monitoring
Die Neurologische Klinik nimmt im Rahmen pharmakologischer Therapiestudien mit MRT-Monitoring in MRT-verantwortlicher Funktion an zahlreichen internationalen Studien teil, insbesondere zur Behandlung der Multiplen Sklerose und dementieller Erkrankungen. Die Neurologische Klinik ist hierbei aufgrund der langjährigen Studien-Expertise für standardisierte MRT-Protokolle als MRT-Zentrum sehr gut eingeführt. Klinisch wurde zusammen mit PD Dr. J. Wagner die Methode der Voxel-basierten 3D-MRT-Analyse in Zusammenarbeit mit Prof. Dr. H.-J. Huppertz angewandt zur automatisierten MRT-Screening-Untersuchung auf kortikale Malformationen/fokale kortikale Dysplasien bei Epilepsie-Syndromen.
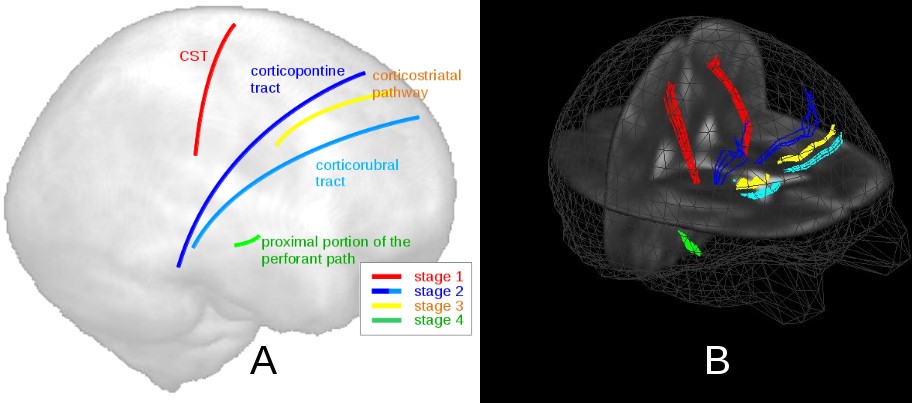
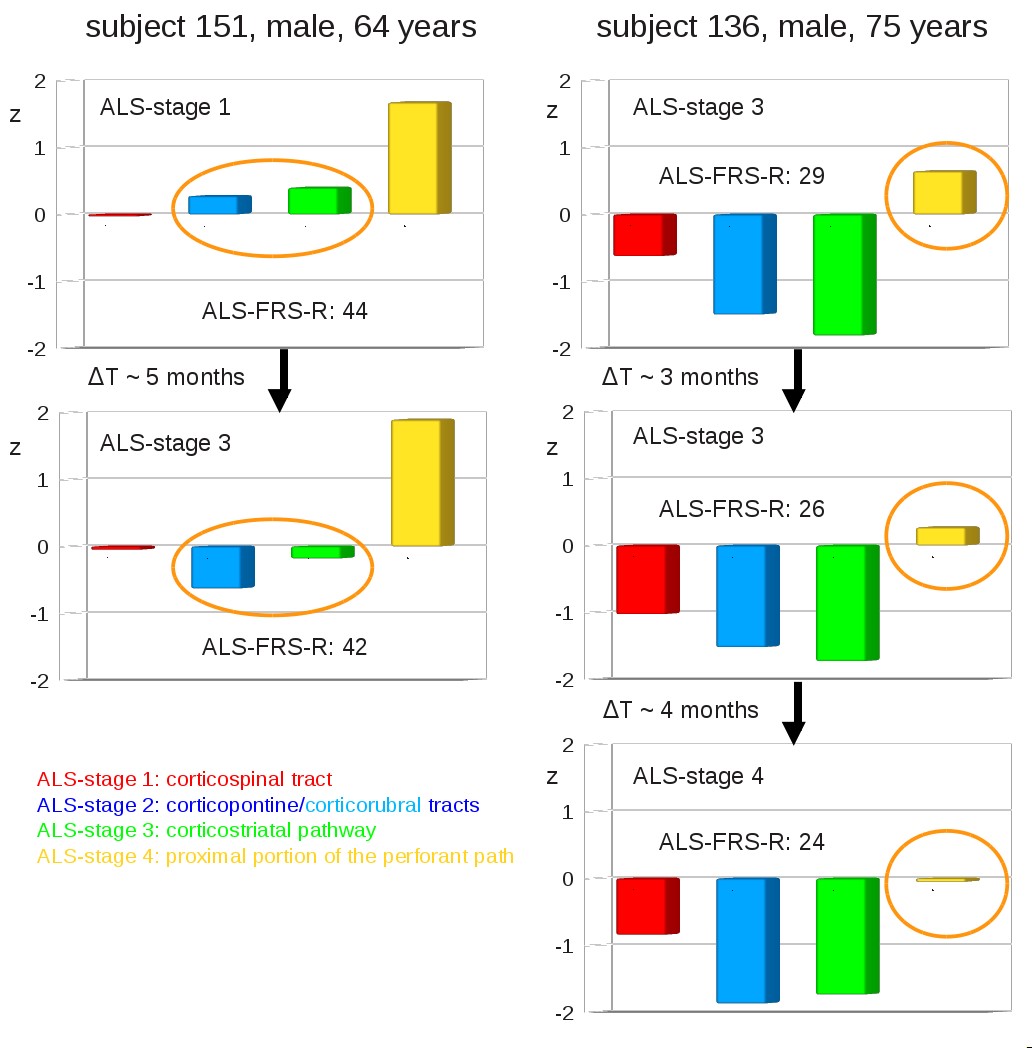
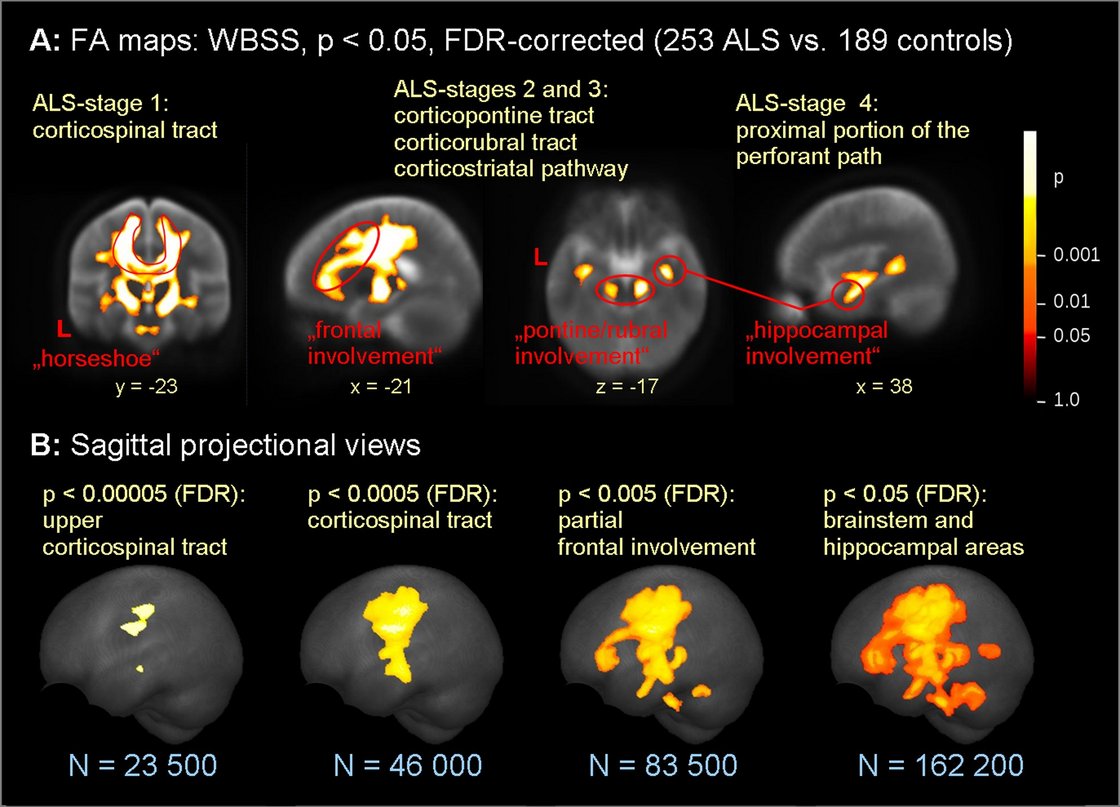
Ein inhaltlicher und methodischer Fokus der AG Neuroimaging ist die klinisch basierte Einzelfallcharakterisierung mittels MRT-Biomarker. Es wurde bei ALS vor dem Hintergrund des neuropathologischen Konzeptes zum Staging die klinisch basierte Einzelfallcharakterisierung mittels traktspezifischer MRT-Biomarker weiter etabliert. Hierbei werden mittels eines spezifischen Algorithmus für die ALS-Stadien 1-4 mit TOI-basiertem Ansatz Trakte definiert, für die dann z-Scores DTI-basierter Metriken auf Individualniveau analysiert werden können.
Diese in vivo-Staging-Prinzipien wurden auf weitere ALS-Varianten wie die progressive Bulbärparalyse (PBP) angewendet, und es konnte in vivo ein Schädigungsmuster der kortikoefferenten Trakte entsprechend dem ALS-Propagations-Modell gezeigt werden. Dieses Ergebnis stützt die Einordnung dieses weiteren ALS-Phänotyps als Variante der ALS und damit die klinische Behandlung dieser Patienten wie bei ALS einschließlich des Einschlusses in klinische Studien zur ALS. Die weitere Anwendung dieses Konzepts erfolgte als vergleichende Analyse von familiären ALS-Formen wie ALS bei c9orf72-Mutation.
In einer durch die Josef und Therese Mayer Stiftung geförderten Studie zur in vivo Krankheitsstadienerfassung bei M. Parkinson (Braak-Stadien) mittels bildgebendem Konzept mit einem Fokus auf kognitive Symptome soll die strukturelle Konnektivität auf Netzwerkebene untersucht werden.
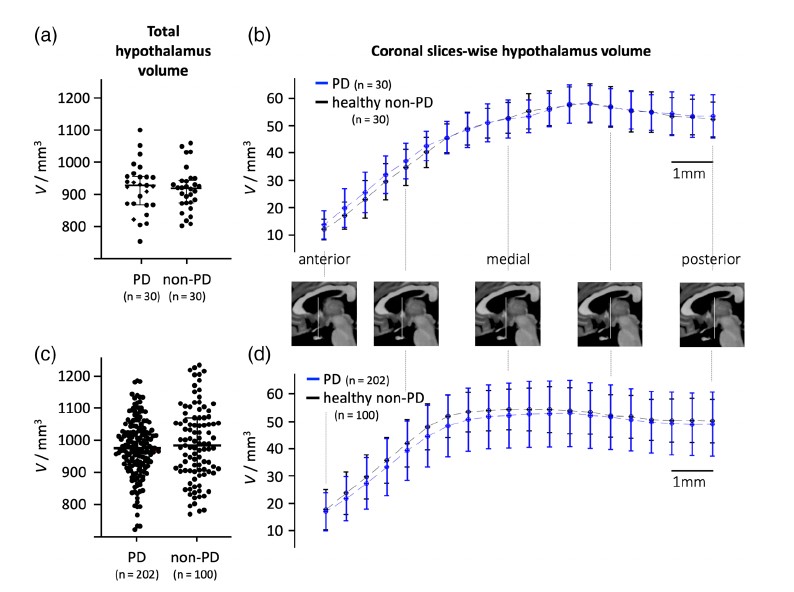
Die Studien in Kooperation mit der AG Neural Networks in Neurology (PD Dr. F. Roselli) mit einem translationalen Ansatz das funktionelle und strukturelle Netzwerk im Menschen und Kleintier dezidiert zu analysieren haben das Ziel ein pathophysiologisches Verständnis der zugrundeliegenden Netzwerkpathologie in einem präsymptomatischen Stadium zu entwickeln.
Die Technik zur Hypothalamussegmentierung wurde auf eine Kohorte von IPS Patienten angewendet und es konnte gezeigt werden, dass bei IPS der Hypothalamus zusammen mit hypothalamisch vermittelten Hormonen keine Veränderungen zeigt (Nachwuchsförderung durch die Deutsche Parkinsongesellschaft e.V.).
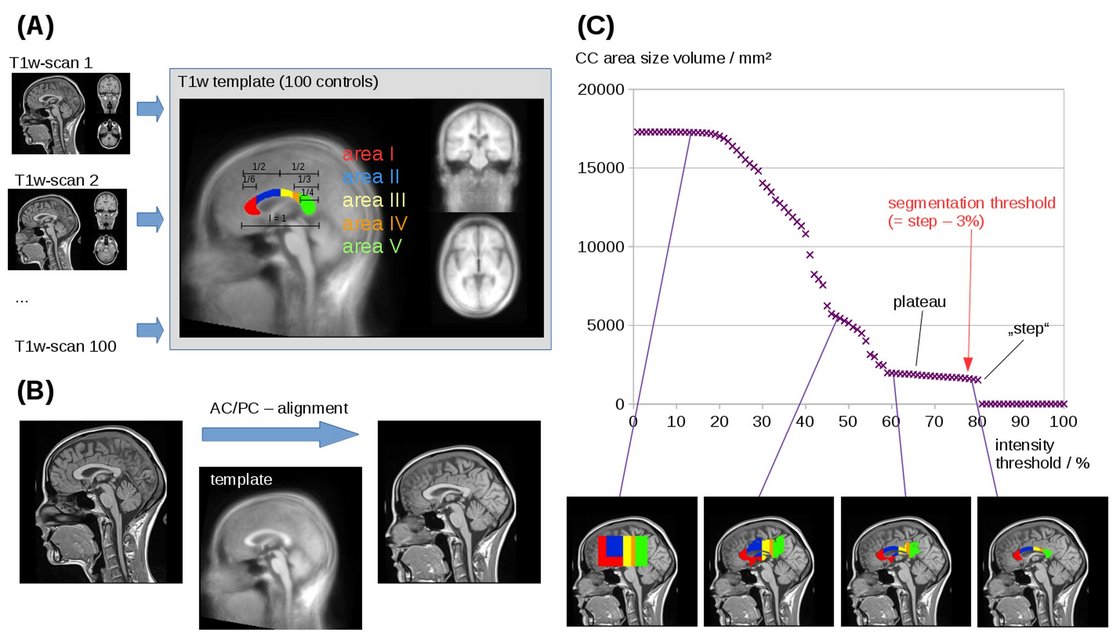
Strukturelle Untersuchungen bei Patienten mit primärer Lateralsklerose (PLS) weisen auf makro- und mikrostrukturelle Veränderungen im Corpus Callosum hin. Diese Veränderungen können mit T1-gewichteter Bildgebung unter Verwendung eines Texturbasierten Mustererkennungsalgorithmus detektiert werden. Es konnte sowohl eine makrostrukturelle Atrophie des Segments 3 des Corpus Callosum (CC) nachgewiesen werden wie auch stukturelle Veränderungen der Texturparameter Entropie und Homogenität.
Diese volumetrischen Analysen zu strukturellen Texturunterschieden zusammen mit den etablierten Analysen der Mikrostruktur via DTI sind wesentliche Elemente zur Entwicklung eines automatischen Analysewerkzeugs, welches es erlauben soll, eine zuverlässige Einteilung von ALS Patienten (inklusive von Varianten) in das Braak-Schema durchzuführen. Dieses Analysewerkzeug wird weiter entwickelt, indem basierend auf Künstlicher Intelligenz (KI) ein „Machine Learning“ (ML)- Algorithmus konditioniert wird, um dann auf ein Analysekollektiv angewendet zu werden.
Das seit dem Jahr 2011 regelmäßig von der AG NeuroImaging organisierte Arbeitsgruppentreffen einer „Tier-MRT-Arbeitsgruppe“ zusammen mit der Arbeitsgruppe von Prof. V. Rasche, Core Facility Small Animal MRI, unter Mitwirkung verschiedener Arbeitsgruppen der Neurologie und anderer Abteilungen des NCU zusammen mit Boehringer Ingelheim Pharma GmbH & Co. KG) ist als „Workgroup Translational Neuroimaging/Tier-MRT“ in das MoMAN-Center for Translational Imaging (https://www.uni-ulm.de/einrichtungen/moman/) integriert.
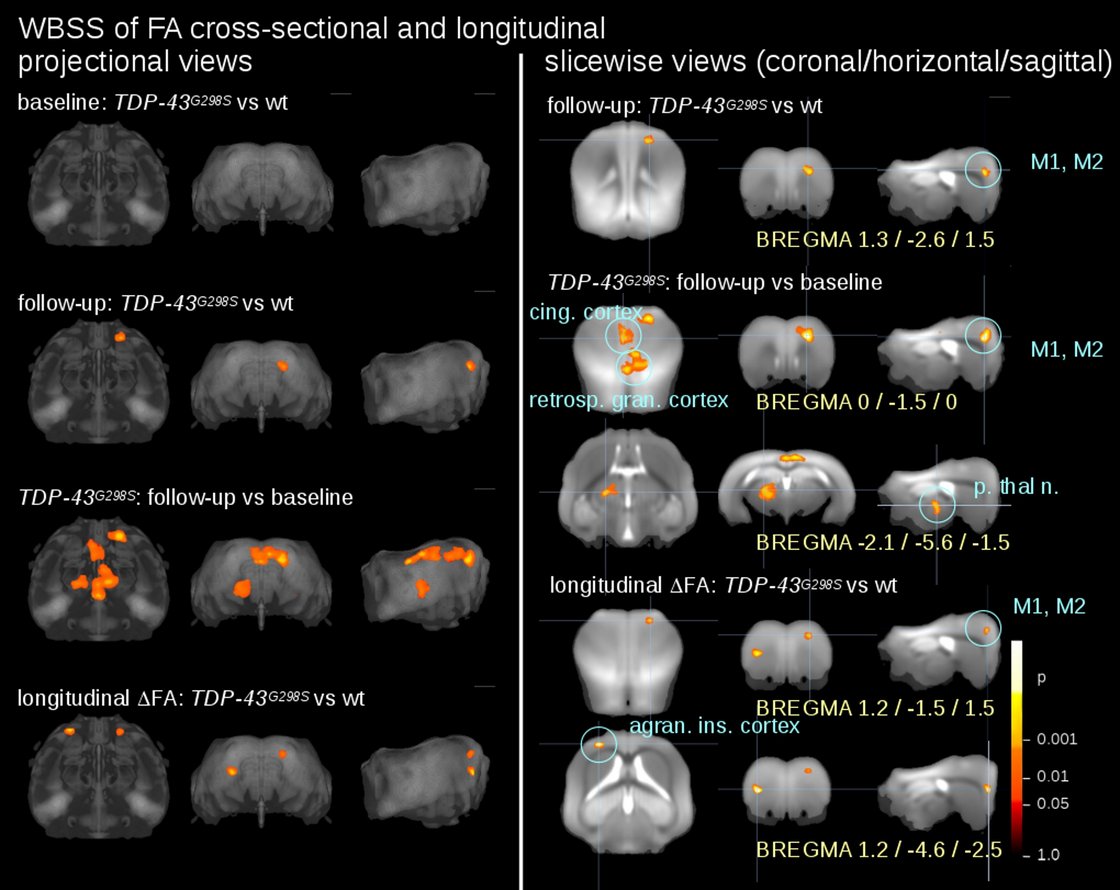
Hauptfokus für die AG NeuroImaging ist hierbei die methodische Etablierung der translationalen DTI-basierten Anwendungen der multiparametrischen Bildgebung in Kombination von DTI mit IFC-MRT. Longitudinale Veränderungsmuster der Mikrostruktur mittels DTI-Methoden in einer Kohorte von 20 Mäusen eines ALS-Modells (TDP43G298S) in Zusammenarbeit mit den AG Weishaupt und Roselli und der Core Facility Small Animal MRI (Prof. V. Rasche) konnten detektiert werden.
In einem gemeinsamen translationalen Projekt zusammen mit Prof. L. Dupuis, Universität Strasbourg, und der AG Neural Networks in Neurology (PD Dr. F. Roselli) wird zudem das Hypothalamus-Konnektom beim ALS-Mausmodell bearbeitet.
In einer Kooperation mit dem Institut für Anatomie und Zellbiologie
Universität Ulm (Prof. Dr. T. Boeckers, Dr. M. Schön) wurden in einem SHANK3-transgenen Mausmodell mit der Tissue Classification Software (TCS) der AG NeuroImaging volumetrisch Veränderungen von Gehirnstrukturen longitudinal untersucht.
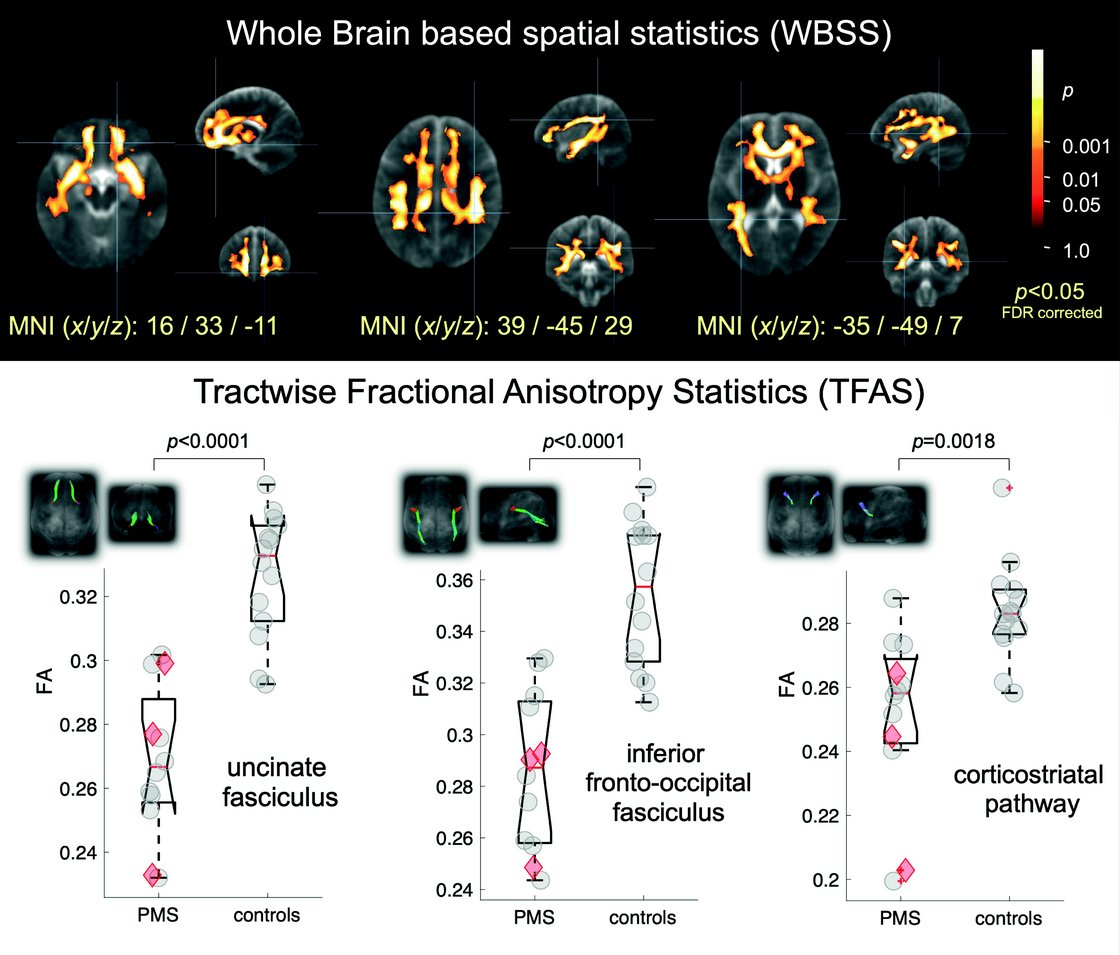
In diesem Zusammenhang wurde in einem translationalen Projekt parallel das in seiner phänotypischen Ausprägung sehr variable humane Phelan-McDermid (PMcD)-Syndrom (orphan disease (OMIN 606232) als SHANK-assoziierte Erkrankung und im translationalen Modell SHANK3-transgene Mäuse untersucht. Mittels DTI konnte gezeigt werden, dass Patienten mit einer genetisch gesicherten Diagnose eines PMcD-Syndroms Veränderungen bzgl. der Mikrostruktur der spezifischen Traktsysteme aufweisen.
