Aktuelle Forschung am Lehrstuhl für Dermatologie und Allergologie
Forschungsschwerpunkte
Schwerpunkte umfassen die Erforschung von Alterungsprozessen der Haut und des Immunsystems. Hierbei spielen die gestörten Zell-Zell und Zell-Matrix Wechselwirkungen aber auch Störungen der Funktion von Stammzellen und residenten Zellen in der Epidermis und Dermis eine bisher wenig geklärte Rolle. Gerade mit der demographisch zunehmenden Alterung der Menschen und unserer Patienten ist das Verständnis grundlegender Mechanismen von Alterungsvorgängen verschiedener Organe, besonders der Haut einschließlich des Immunsystems von hervorragender Bedeutung. Dies deshalb, weil es durch Störungen von Signalwegen bei Alterungsprozessen für Wundheilungsstörungen, Verlust an Regenerationsfähigkeit und durch Immunseneszenz vermehrt zu allergischen Reaktionen und zu Autoimmunerkrankungen (darunter bullöse Dermatosen, Psoriasis vulgaris, Autoimmun- Erkrankungen aus dem Formenkreis der Kollagenosen), Infektionen und malignen Tumoren kommt. Gerade in der letzten Zeit wird zunehmend deutlich, dass aus dem Bindegewebe freigesetzte Substanzen (Seneszenz-assoziierter sekretorischer Phänotyp) und die Immunseneszenz - zusätzlich zu autologen Mutationen von Tumorzellen - die Progression von malignen Tumorender Haut (malignes Melanom, spinozelluläres Karzinom, kutane Lymphome) fördern. Zur Erforschung werden zell- und molekularbiologische sowie biochemische Ansätze verfolgt. Wir verfügen über sehr gut ausgestattete Laboratorien mit enger Anbindung an vorklinische Institute und zentrale Einrichtungen, die über State-of-the-Art Technologien verfügen.
In der Klinik/Lehrstuhl für Dermatologie und Allergologie in Ulm versuchen wir durch die Erforschung von grundlegenden Mechanismen neue Behandlungen in die Klinik zu bringen, und umgekehrt klinische Beobachtungen im Labor aufzuschlüsseln, um über ein verbessertes Verständnis der Pathogenese neue präventive und therapeutische Ansätze für unsere Patienten zu entwickeln. Zudem sind 2 klinische Studienzentren aktiv, um neue therapeutische Strategien in multizentrischen Studien zu überprüfen, und Nebenwirkungen moderner zielgerichteter Therapien zu verbessern.
Die Klinik hat ein besonderes Interesse an einer kliniknahen Forschung und der interdisziplinären Vernetzung mit Nachbardisziplinen. Es werden neueste zielgerichtete Therapien für die entzündlichen und malignen Erkrankungen der Haut (Psoriasis, atopische Dermatitis, Autoimmunerkrankungen, Autoinflammations-Syndrome, maligne Tumoren und Lymphome) in der Klinik durchgeführt, weiterentwickelt und für neue Indikationen eingesetzt.
Arbeitsgruppen
Im Folgenden werden die Arbeitsgruppen und deren Schwerpunkte näher erläutert:
Arbeitsgruppe Prof. Karin Scharffetter-Kochanek
Arbeitsgruppe Professor Dr. med. Johannes Weiss
Arbeitsgruppe Priv.-Doz. Dr. med. Sebastian Iben
Arbeitsgruppe Priv.-Doz. Dr. med. Anca Sindrilaru
Arbeitsgruppe Priv.-Doz. Dr. med. Christiane Pfeiffer
Arbeitsgruppe Priv.-Doz. Dr. med. Thorsten Peters
An den Lehrstuhl für Dermatologie und Allergologie angeschlossene externe Professoren
Prof. Dr. med. Lars-Alexander Schneider (Ulm)
Prof. Dr. med. Margit Huber (Landshut)
Arbeitsgruppe Prof. Karin Scharffetter-Kochanek

Prof. Scharffetter-Kochanek

Dr. rer. nat. Meinhard Wlaschek (Laborleiter)

Dr. Pallab Maity, Ph.D.

Dr. Karmveer Singh, Ph.D.

Dr. Evgenia Makrantonaki

Dr. Philipp Haas, Ph.D.

Dr. Albert Koroma, Ph.D.

Jinnan Cheng, medizinischer Doktorand

Heidi Hainzl, ltd technische Assistentin

Susanne Schatz, technische Assistentin

Linda Krug, technische Assistentin
ALTERUNG DER HAUT
Fibroblastenseneszenz (Dr. Pallab Maity, Dr. Karmveer Singh, Linda Krug, Heidi Hainzl, Dr. Meinhard Wlaschek)
Die Haut gilt als „Markerorgan“ für die Alterung innerer Organe. Wir verfolgen die Hypothese, dass der Alterung des Bindegewebes mit den darin angesiedelten Fibroblasten eine wesentliche Bedeutung bei der Alterung von Organen und des gesamten Organismus zukommt.
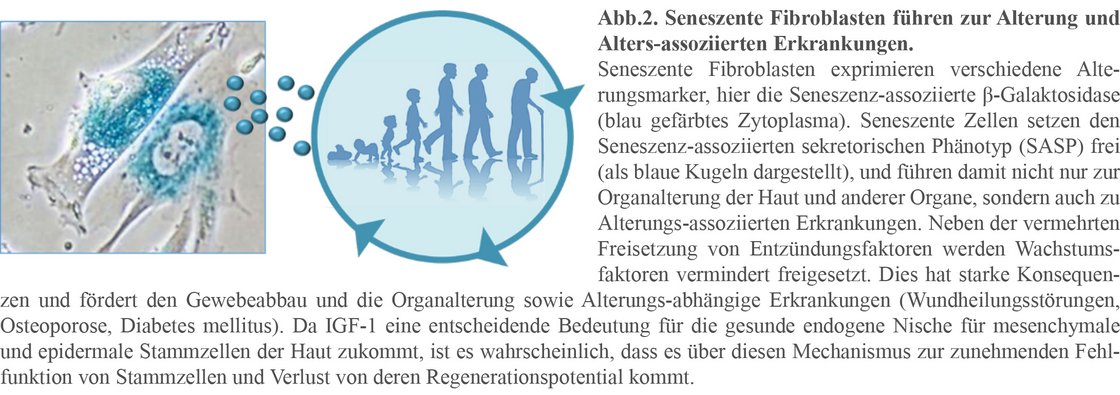
Fibroblasten gehen, wenn diese molekulare Schäden ihrer DNA aufweisen, nicht in die Apoptose, sondern aktivieren Zellzyklus-Checkpunkte wie p16, die zur Aktivierung eines irreversiblen Seneszenzprogrammes mit vollständigem Wachstumsarrest führen. Das bedeutet, dass die seneszenten Fibroblasten sich in der Dermis anhäufen und über die Freisetzung von pro-inflammatorischen Zytokinen, Chemokinen sowie Matrix-abbauenden Metalloproteasen (Seneszenz-assoziierter sekretorischer Phänotyp - SASP) kommt es zur Veränderung der endogenen Nische und zur Alterung auch anderer Gewebe der Haut, wie beispielsweise der Epidermis, des subkutanen Bindegewebes und der Haarfollikel. In den letzten Jahren konnten wir einen Transkriptionsfaktor identifizieren, der die Seneszenz der Fibroblasten vermittelt und gleichzeitig für die Unterdrückung des Wachstumsfaktors Insulin Wachstumsfaktor-1 (IGF-1) verantwortlich ist.
Ungelöste Fragen: Den Konsequenzen einer längerfristigen Aktivierung des Transkriptionsfaktors für die Fibroblasten-spezifische Seneszenz untersuchen wir derzeit in der Haut des Menschen. Zudem möchten wir Inhibitoren des Transkriptionsfaktors entwickeln, die ausschließlich in seneszenten Fibroblasten zur Wirkung kommen. Die Neutralisierung einzelner Faktoren des sekretorischen Phänotyps von seneszenten Fibroblasten könnte auch für den Erhalt des Gewebes interessant sein. Ebenso werden Senolytika, Substanzen die spezifisch zum Zelltod von seneszenten Zellen führen, von uns und zahlreichen Forschern als Anti-Aging-Konzept verfolgt. In murinen Modellen konnten Wissenschaftler bereits eine Verjüngung von alternden Organen durch Depletion von seneszenten Zellen zeigen. Das wäre sehr interessant, da seneszente Fibroblasten nicht nur für den Alterungsphänotyp, sondern auch für die Ausbreitung von Tumoren, Wundheilungsstörungen und vermutlich Alterung und Erkrankungen anderer Organe verantwortlich sind.
Immunseneszenz bei Alterungsvorgängen der Haut(Albert Koroma, Ph.D. Student, Dr. Pallab Maity)
Bei physiologischen Prozessen in der Embryogenese und der akuten Wundheilung kommt es durchaus zum Auftreten von seneszenten Zellen und Fibroblasten, die sehr effektiv von Zellen des nativen Immunsystems abgeräumt werden. Diese effektive Abräumung von seneszenten Zellen findet in alternden Geweben nicht oder vermindet statt. Dadurch kommt es zur Persistenz von seneszenten Zellen, die lösliche Faktoren wie beispielsweise Chemokine, Zytokine, Matrix-abbauende Metalloproteinasen und andere freigesetzen. Diese löslichen Faktoren gehören zum Seneszenz-assoziierten sekretorischen Phänotyp (SASP). Durch den von Fibroblasten freigesetzten SASP kann Seneszenz auch an benachbarte Zellen weitergegeben werden, und es kommt zur Desintegration des Gewebes der Haut und vermutlich anderer Organe.
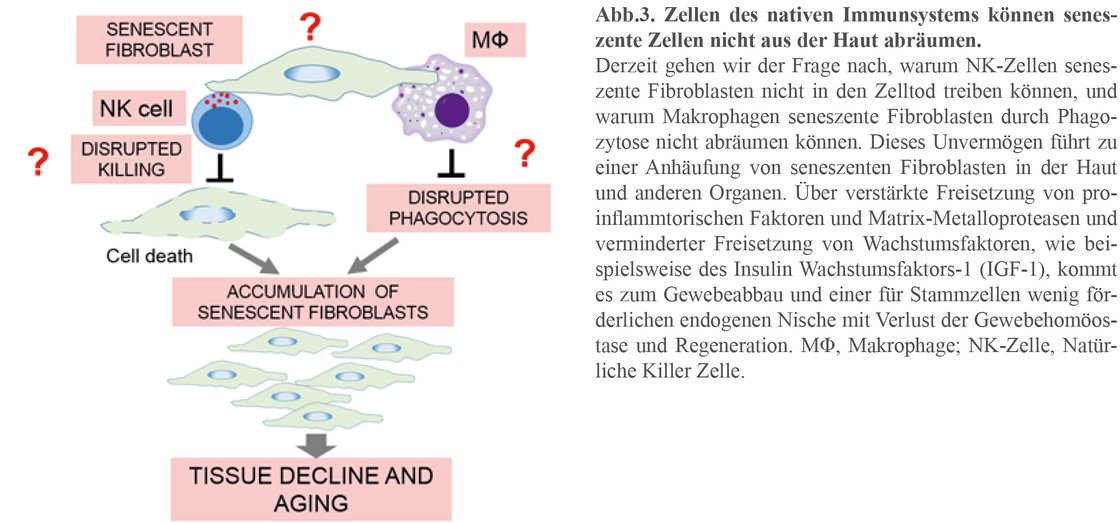
Wir interessieren uns dafür, ob im Rahmen der Immunseneszenz die Makrophagen (MΦ) und Natürliche Killerzellen (NK-Cells) nicht mehr in der Lage sind, seneszente Fibroblasten aus dem Gewebe abzuräumen, oder ob seneszente Fibroblasten selber die Immunzellen am Abräumen hemmen. Hierzu werden derzeit Techniken in Zellkultur mit Analysen der Perforin und Granzym aber auch Phagozytose-Aktivität der Zellen des nativen Immunsystems untersucht. Ebenso werden murine Modelle mit defizienten NK-Zellen und Makrophagenpopulationen charakterisiert, um die in vivo-Bedeutung dieser Zellen bei der Abräumung seneszenter Zellen besser verstehen zu lernen.
Ungelöste Fragen: Kann die Aktivierung von Zellen des nativen Immunsystems zur besseren Abräumung von seneszenten Zellen und damit zur Prävention der Gewebealterung führen? Ist es denkbar eine Zell-basierte Therapie mit jungen oder pharmakologisch behandelten autologen Zellen des nativen Immunsystems erfolgreich durchzuführen, um seneszente Zellen aus dem Gewebe zu entfernen?
Zhang Y, Guo P, Xiang W, Liu Q, Liu X, Ma N, Zhou S, He H, Wlaschek M, Scharffetter-Kochanek K, Zhang TC, Ma W. (2020) Slowly Repaired Bulky DNA Damages Modulate Cellular Redox Environment Leading to Premature Senescence. Oxid Med Cell Longev. doi: 10.1155/2020/5367102
Singh K, Camera E, Krug L, Basu A, Kumar Pandey R, Munir S, Wlaschek M, Kochanek S, Schorpp-Kistner M, Picardo M, Angel P, Niemann C, Maity P, Scharffetter-Kochanek (2018) JunB defines functional and structural integrity of the epidermo-pilosebaceous unit in the skin. Nature Commun. 9:3425 | DOI: 10.1038/s41467-018-05726-z.
Meyer P, Maity P, Burkovski A, Schwab J, Müssel C, Singh K, Ferreira FF, Krug L, Maier HJ, Wlaschek M, Wirth T, Kestler HA, Scharffetter-Kochanek K. (2017) A model of the onset of the senescence associated secretory phenotype after DNA damage induced senescence. PLoS Comput Biol. 13:e1005741.
Singh K, Maity P, Krug L, Meyer P, Treiber N, Lucas T, Basu A, Kochanek S, Wlaschek M, Geiger H, Scharffetter-Kochanek K. (2015) Superoxide anion radicals induce IGF-1 resistance through concomitant activation of PTP1B and PTEN. EMBO Mol Med 7(1):59-77.
Treiber N, Maity P, Singh K, Kohn M, Keist AF, Ferchiu F, Sante L, Frese S, Bloch W, Kochanek S, Sindrilaru A, Iben S, Högel J, Ohnmacht M, Claes LE, Ignatius A, Chung JH, Lee MJ, Kamenisch Y, Berneburg M, Nikolaus T, Braunstein K, Sperfeld AD, Ludolph AC, Briviba K, Wlaschek M, Scharffetter-Kochanek K. (2011) Accelerated aging phenotype in mice with conditional deficiency for mitochondrial superoxide dismutase in the connective tissue. Aging Cell. 10:239-254
Briganti S, Wlaschek M, Hinrichs C, Bellei B, Flori E, Treiber N, Iben S, Picardo M, Scharffetter-Kochanek K. (2008) Small molecular antioxidants effectively protect from PUVA-induced oxidative stress responses underlying fibroblast senescence and photoaging. Free Radic Biol Med. 45: 636-644.
Peters T, Weiss JM, Sindrilaru A, Wang H, Oreshkova T, Wlaschek M, Maity P, Reimann J, Scharffetter-Kochanek K. (2009) Reactive oxygen intermediate-induced pathomechanisms contribute to immunosenescence, chronic inflammation and autoimmunity. Mech Ageing Dev. 130(9):564-87.
Ressler S, Bartkova J, Niederegger H, Bartek J, Scharffetter-Kochanek K, Jansen-Dürr P, Wlaschek M. (2006) p16INK4a qualifies as a robust biomarker of cellular aging in human skin. Aging Cell. 5:379-390.
Wenk J, Schüller J, Hinrichs C, Syrovets T, Azoitei N, Podda M, Wlaschek M, Brenneisen P, Schneider LA, Sabiwalsky A, Peters T, Sulyok S, Dissemond J, Schauen M, Krieg T, Wirth T, Simmet T, Scharffetter-Kochanek K. (2004) Overexpression of phospholipid hydroperoxide glutathione peroxidase in human dermal fibroblasts abrogates UVA-induced expression of interstitial collagenase/matrix-metalloproteinase-1 by suppression of phosphatidylcholine hydroperoxide-mediated NFkappa B activation and interleukin-6 release. J Biol Chem. 279:45634-42.
Ma W, Wlaschek M, Hommel C, Schneider LA, Scharffetter-Kochanek K (2002) Psoralen plus UVA (PUVA) induced premature senescence as a model for stress-induced premature senescence. Exp Gerontol. 37: 1197-1120.
Ma W, Wlaschek M, Brenneisen P, Schneider LA, Hommel C, Hellweg C, Sauer H, Wartenberg M, Herrmann G, Scharffetter-Kochanek K (2001) Chrono- and photoaging of the fibroblast and the dermal connective tissue. Clin Exp Dermatol. 26: 592-599.
Brenneisen P, Wenk J, Wlaschek M, Krieg T, Scharffetter-Kochanek K. (2000) Activation of p70 ribosomal protein S6 kinase is an essential step in the DNA damage-dependent signaling pathway responsible for the ultraviolet B-mediated increase in interstitial collagenase (MMP-1) and stromelysin-1 (MMP-3) protein levels in human dermal fibroblasts. J Biol Chem. 275: 4336-4344.
Wenk J, Brenneisen P, Wlaschek M, Poswig A, Briviba K, Oberley TD, Scharffetter-Kochanek K (1999) Stable overexpression of manganese superoxide dismutase in mitochondria identifies hydrogen peroxide as a major oxidant in the AP-1 mediated induction of matrix-metalloprotease-1/MMP-1. J Biol Chem. 274: 25869-25876
Brenneisen P, Wenk J, Klotz OL, Wlaschek M, Briviba K, Krieg T, Sies H, Scharffetter-Kochanek K (1998) Central role of ferrous/ferric iron in the ultraviolet B irradiation-mediated signaling pathway leading to increased interstitial collagenase (matrix-degrading metalloprotease (MMP)-1) and stromelysin-1 (MMP-3) mRNA levels in cultured human dermal fibroblasts. J Biol Chem. 273: 5279-5287.
Wlaschek M, Briviba K, Stricklin GP, Sies H, Scharffetter-Kochanek K (1995) Singlet oxygen may mediate the ultraviolet A induced synthesis of interstitial collagenase. J Invest Dermatol. 104: 194-198
Die Bedeutung der seneszenten Fibroblasten bei der Progression von malignen Tumoren der Haut (Dr. Abhijit Basu, Dr. Vida Farsam (Alumna), Susanne Schatz)
Neben Mutationen von Keratinozyten und Melanozyten, die während der Onkogenese zu malignen Tumoren wie dem spinozellulären Karzinom und dem malignen Melanom führen, ist zunehmend die Bedeutung des peritumoralen Bindegewebes in den Blickpunkt der Forschung gerückt.In der Klinik für Dermatologie und Allergologie am Universitätsklinikum Ulm gehen wir der Frage nach, wie seneszente Fibroblasten die Tumorprogression von spinozellulären Karzinomen und beim malignen Melanom beeinflussen. Dabei interessiert uns besonders die Freisetzung von Faktoren des Seneszenz-assoziierten sekretorischen Phänotyps (SASP) der alten Fibroblasten. Mittels Antikörper-Arrays und RNA Seq Technologie konnten wir den SASP des seneszenten Fibroblasten aufklären. So identifizierten wir das von seneszenten Fibroblasten freigesetzte Chemerin, ein Chemokin, welches über Bindung an korrespondierende Rezeptoren der malignen spinozellulären Karzinomzellen über den MAP/Jun Kinase Signalweg deren Wanderung und Invasion in das dermale Bindegewebe befördert.
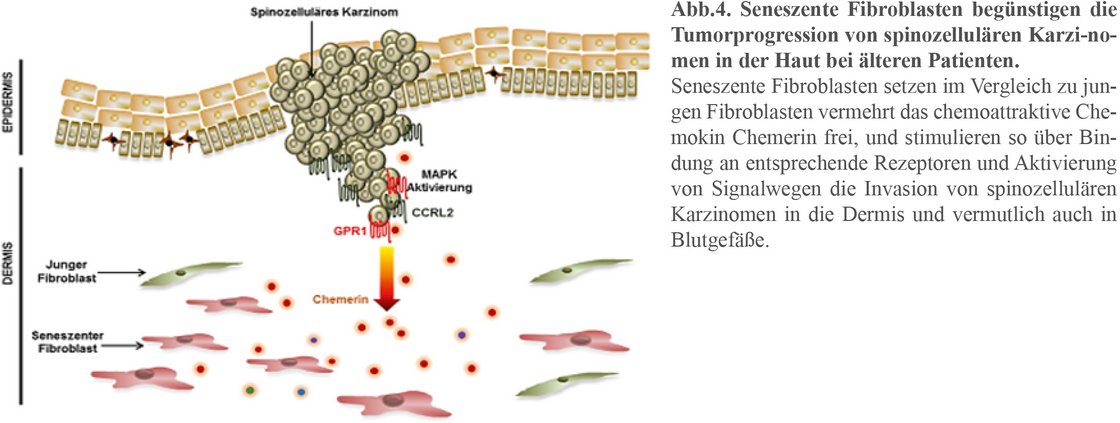
Auch konnte ein Set von Chemokinen herausgearbeitet werden, welches die Migration, die Invasion und das Wachstum von primären Melanomzellen und Melanomzelllinien in vitro und in vivo an präklinischen Modellen induziert. Die identifizierten Chemokine wurden auch an Gewebe von spinozellulären Karzinomen und Melanomen älterer Patienten, nicht jedoch jüngerer Patienten nachgewiesen. Diese Daten zeigen, dass dem peritumoralen Bindegewebe eine zentrale, bisher wenig erforschte Rolle bei der Progression von malignen Hauttumoren zukommt.
Ungelöste Fragen: Es werden nun die Signalwege dieser durch seneszente Fibroblasten freigesetzten Chemokine aufgeklärt, um den Signalweg therapeutisch gezielt zu unterbrechen. Dieses Vorgehen wird langfristig präventive und therapeutische Ansätze ermöglichen.
Farsam V, Basu A, Gatzka M, Treiber N, Schneider LA, Mulaw MA, Lucas T, Kochanek S, Dummer R, Levesque MP, Wlaschek M, Scharffetter-Kochanek K. (2016) Senescent fibroblast-derived Chemerin promotes squamous cell carcinoma migration. Oncotarget. 7:83554-83569
Meyer P, Maity P, Burkovski A, Schwab J, Müssel C, Singh K, Ferreira FF, Krug L, Maier HJ, Wlaschek M, Wirth T, Kestler HA, Scharffetter-Kochanek K. (2017) A model of the onset of the senescence associated secretory phenotype after DNA damage induced senescence. PLoS Comput Biol. 13:e1005741.
Mesenchymale Stammzellen bei Alterungsvorgängen (Philipp Haas, Ph.D. Student, Dr. Karmveer Singh, Dr. Juliane de Vries (Alumna), Dr. Seppe Vander Beken (Alumnus), Heidi Hainzl)
Die ABCB5+ MSC haben eine Präferenz in ihrer endogenen Nische. Entweder sie halten sich in der Nähe von Gefäßen oder in der interstitiellen Dermis auf. Derzeit untersuchen wir, ob diese Subpopulation - ähnlich wie bei aus Fettgewebe abgeleiteten MSC - durch das Transkriptionsprogramm nach Exposition mit dem Bakterienwandbestandteil LPS (Lipopolysaccharid) verändert werden kann. Zudem gehen wir der Frage nach, ob dieses „Priming“ der LPS vorbehandelten ABCB5+ MSC vor Transplantation auch zur Verbesserung der Wundheilung in präklinischen Modellen führt.
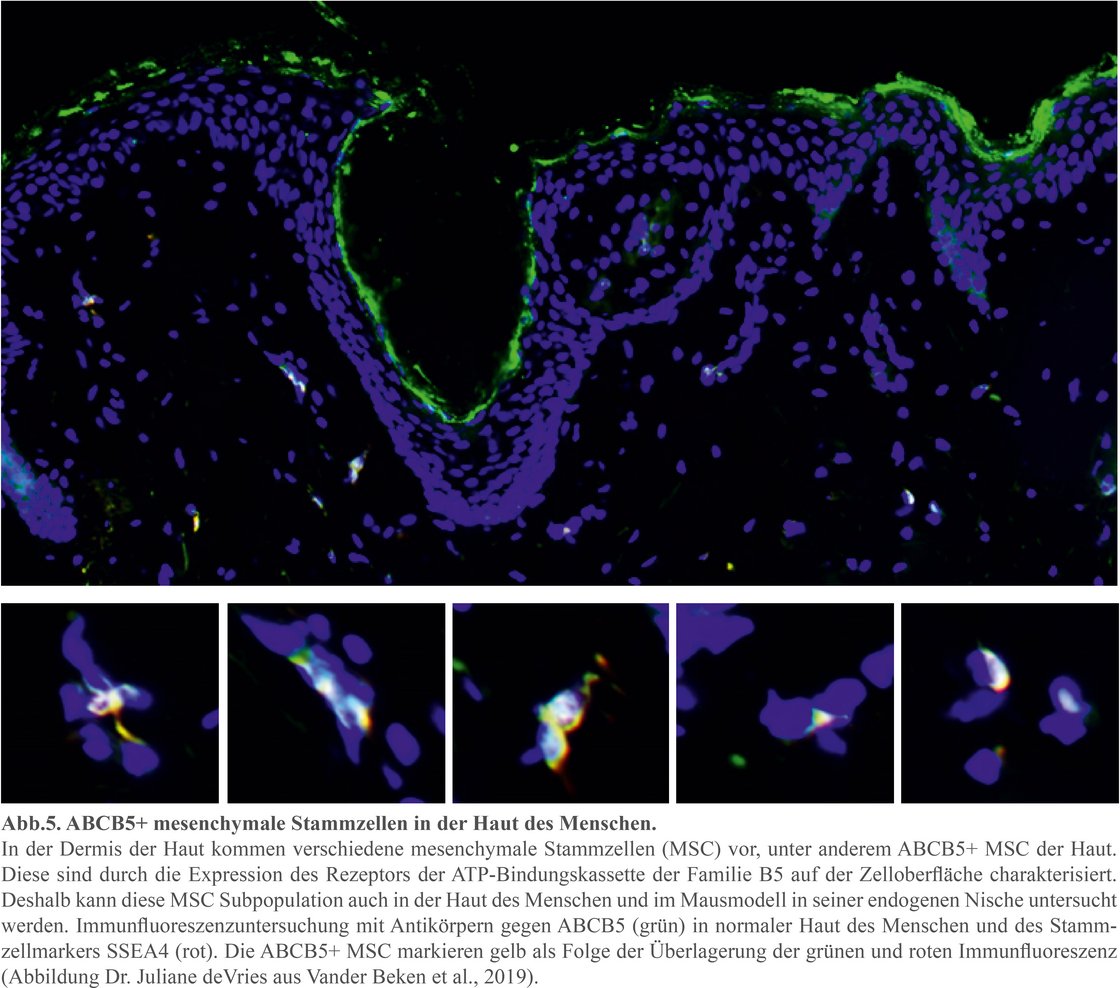
Dies haben wir für aus Fettgewebe stammenden MSC beobachtet (Munir, Basu et al., 2020). In der Dissertation von Herrn Philipp Haas wird der Frage nachgegangen, ob auch die ABCB5+ MSC zu dieser adaptiven Antwort mit rascher Umstellung des Transkriptoms befähigt sind und, ob ABCB5+ MSC von jungen und alten Spendern unterschiedlich reagieren. Dies könnte klinisch von Bedeutung sein, wenn ältere Spender das Transkriptom qualitativ und quantitativ weniger gut auf LPS anpassen könnten und damit vermutlich weniger gut auf Infektionen reagieren könnten. Letztlich werden Ergebnisse dieser Forschungsrichtung der adaptiven Antworten von mesenchymalen Stammzellen auch helfen, die MSC-basierten Therapien zur Behandlung von infizierten Wunden und chronischen Wunden zu verbessern und klinisch zu nutzen.
Ungelöste Fragen: Wie kann die endogene Niche manipuliert werden, dass die Geweberegeneration und Wundheilung der mesenchymalen Stammzellen besser charakterisiert werden, und wie kann die endogene Niche manipuliert werden das die Geweberegeneration und Wundheilung beeinflusst werden können. Suche nach Möglichkeiten die Stammzelltherapien zu verbessern.
Jiang D, Singh K, Muschhammer J, Schatz S, Sindrilaru A, Makrantonaki E, Qi Y, Wlaschek M, Scharffetter-Kochanek K. MSCs rescue impaired wound healing in a murine LAD1 model by adaptive responses to low TGF-β1 levels. EMBO Rep. 2020 Feb 21:e49115. [Epub ahead of print]
Munir S, Basu A, Maity P, Krug L, Haas P, Jiang D, Strauss G, Wlaschek M, Geiger H, Singh K, Scharffetter-Kochanek K. TLR4-dependent shaping of the wound site by MSCs accelerates wound healing. EMBO Rep. 2020 Mar 12:e48777. doi: 10.15252/embr. 201948777. [Epub ahead of print]
Jiang and Scharffetter-Kochanek (2020) Mesenchymal stem cells adaptively respond to environmental cues thereby improving granulation tissue formation and wound healing. Front Immunol. [submitted.
Vander Beken S, de Vries JC, Meier-Schiesser B, Meyer P, Jiang D, Sindrilaru A, Ferreira FF, Hainzl A, Schatz S, Muschhammer J, Scheurmann NJ, Kampilafkos P, Seitz AM, Dürselen L, Ignatius A, Kluth MA, Ganss C, Wlaschek M, Singh K, Maity P, Frank NY, Frank MH, Scharffetter-Kochanek K. (2019) Newly Defined ATP-binding cassette subfamily B member 5 Positive Dermal Mesenchymal Stem Cells Promote Healing of Chronic Iron-Overload Wounds via Secretion of Interleukin-1 Receptor Antagonist. Stem Cells. 37:1057-1074.
Basu A, Munir S, Mulaw MA, Singh K, Herold B, Crisan D, Sindrilaru A, Treiber N, Wlaschek M, Huber-Lang M, Gebhard F, Scharffetter-Kochanek K. (2018) A Novel S100A8/A9 Induced Fingerprint of Mesenchymal Stem Cells associated with Enhanced Wound Healing. Sci Rep. 8:6205.
Jiang D, Muschhammer J, Qi Y, Kügler A, de Vries JC, Saffarzadeh M, Sindrilaru A, Vander Beken S, Wlaschek M, Kluth AM, Ganss C, Frank NY, Frank MH, Preissner KT, Scharffetter-Kochanek K. (2016). Suppression of neutrophil-mediated tissue damage - a novel skill of mesenchymal stem cells. Stem Cells. 34:2393-40.
Jiang D and Scharffetter-Kochanek K (2015) Mesenchymal Stem Cells in Wound Repair, Tissue Homeostasis, and Aging. In: Geiger H, Jasper H, Florian MC (eds) Stem Cell Aging: Mechanisms, Consequences, Rejuvenation. Springer, Vienna Heidelberg New York, pp 287-318.
Schatton T, Yang J, Kleffel S, Uehara M, Barthel SR, Schlapbach C, Zhan Q, Dudeney S, Mueller H, Lee N, de Vries JC, Meier B, Vander Beken S, Kluth MA, Ganss C, Sharpe AH, Waaga-Gasser AM, Sayegh MH, Abdi R, Scharffetter-Kochanek K, Murphy GF, Kupper TS, Frank NY, Frank M. (2015) ABCB5 identifies immunoregulatory dermal cells. Cell Rep. 12:1-11.
Qi Y, Jiang D, Sindrilaru A, Stegemann A, Schatz S, Treiber N, Rojewski M, Schrezenmeier H, Vander Beken S, Wlaschek M, Böhm M, Seitz A, Scholz N, Dürselen L, Brinckmann J, Ignatius A, Scharffetter-Kochanek K. (2014) TSG-6 Released from Intradermally Injected Mesenchymal Stem Cells Accelerates Wound Healing and Reduces Tissue Fibrosis in Murine Full-Thickness Skin Wounds. J Invest Dermatol. 134: 526-537.
Jiang D, Qi Y, Walker N, Sindrilaru N, Hainzl A, Wlaschek M, MacNeil S, Scharffetter-Kochanek K. (2013) The Effect of Adipose Tissue Derived MSCs Delivered by a Chemically Defined Carrier on Full-Thickness Cutaneous Wound Healing. Biomaterials. 34:2501-15.
Florian MC, Nattamai KJ, Dörr K, Marka G, Uberle B, Vas V, Eckl C, Andrä I,Schiemann M, Oostendorp RA, Scharffetter-Kochanek K, Kestler HA, Zheng Y, Geiger H. (2013) A canonical to non-canonical Wnt signalling switch in haematopoietic stem-cell ageing. Nature. 503:392-6.
Florian MC, Dörr K, Niebel A, Daria D, Schrezenmeier H, Rojewski M, Filippi MD, Hasenberg A, Gunzer M, Scharffetter-Kochanek K, Zheng Y, Geiger H. (2012) Cdc42 Activity Regulates Hematopoietic Stem Cell Aging and Rejuvenation. Cell Stem Cell 10:520-530
URSACHEN VON CHRONISCHEN WUNDEN UND DEREN BEHANDLUNG MIT MESENCHYMALEN STAMMZELLEN
(PD Dr. Anca Sindrilaru,Dr. Seppe Vander Beken (Alumnus), Dr. Juliane de Vries (Alumna), Dr. Abhijit Basu, Dr. Karmveer Singh, Dr. Pallab Maity, Dr. Dongsheng Jiang (Alumnus), cand. med. Oliver Storz, Heidi Hainzl, Linda Krug, Susanne Schatz)
Unser Interesse gilt seit vielen Jahren Wundheilungsstörungen, deren Ursache und neuen therapeutischen Möglichkeiten. Chronische Wunden nehmen mit zunehmendem Alter bis zu 4 bis 5 % deutlich zu und betreffen bereits jetzt einen großen Teil unserer Bevölkerung. Wir konnten zeigen, dass chronische Wunden durch eine persistierende Entzündungsreaktion bedingt werden (Wlaschek und Scharffetter-Kochanek, 2005, Wlaschek et al., 2019, Sindrilaru et al., 2011). Der Prozess der Wundheilung kann von dieser Entzündungsphase nicht in die nächste Phase der Wundheilung übergehen. Dieses Nicht-Umschalten von der Entzündungsphase in die Phase der Bildung von Granulationsgewebe (Ersatzgewebe) ist ursächlich für verschiedene chronische Wunden wie das venöse Ulcus, das diabetische Fußulkus (Mal perforans) und das Dekubitalulkus. Dabei spielt eine Überladung von Eisen, auch die sich unter oxidativem Stress entwickelnde Insulinresistenz eine entscheidende Rolle. Wir haben uns in den letzten Jahren mit der Frage beschäftigt, ob mesenchymale Stammzellen die spezifische und unterschiedliche Situation unterschiedlicher Wunden über bestimmte „Sensing-Mechanismen“ erfassen können und ihr Transkriptom sehr rasch an die jeweilige Situation anpassen können. Dieser Hypothese sind wir in akuten und einer Reihe von chronischen Wundmodellen nachgegangen. Das besondere dieser Wundmodelle ist, das diese Pathogenese eines chronisch venösen Ulkus, eines diabetischen Ulcus, einer infizierten Umgebung, einer Vaskulitis nachahmen können. Interessant ist, dass diese unterschiedlichen Situationen sehr spezifische Transkriptomänderungen der MSC bewirken, und diese dann über die Freisetzung von löslichen Faktoren auf verschiedene Zellen wirken, und entscheidend den verzögerten Prozess der Wundheilung beschleunigen können (Qi et al. 2014, Jiang et al., 2013, 2016, Jiang und Scharffetter-Kochanek 2016, 2020). Dieses Sensing der Umgebung mit einer jeweils unterschiedlichen MSC-Antwort ist vermutlich ein evolutionär optimierter Prozess, der den MSC dazu dient, die unterschiedlich feindlichen Bedingungen in ihrer Nachbarschaft zu entschärfen, um deren DNA zu schützen. Denn die Selbsterneuerung der MSC ist auf eine intakte DNA als Blueprint für die Tochterzellen mit Selbsterneuerungspotential angewiesen.
Makrantonaki E, Jiang D, Hossini AM, Nikolakis G, Wlaschek M, Scharffetter-Kochanek K, Zouboulis CC. (2016) Diabetes mellitus and the skin. Rev Endocr Metab Disord. 17:269-282.
Jiang D, Muschhammer J, Qi Y, Kügler A, de Vries JC, Saffarzadeh M, Sindrilaru A, Vander Beken S, Wlaschek M, Kluth AM, Ganss C, Frank NY, Frank MH, Preissner KT, Scharffetter-Kochanek K. (2016). Suppression of neutrophil-mediated tissue damage - a novel skill of mesenchymal stem cells. Stem Cells. 34:2393-40.
Jiang D, Qi Y, Walker N, Sindrilaru N, Hainzl A, Wlaschek M, MacNeil S, Scharffetter-Kochanek K. (2013) The Effect of Adipose Tissue Derived MSCs Delivered by a Chemically Defined Carrier on Full-Thickness Cutaneous Wound Healing. Biomaterials. 34:2501-15.
Jiang D and Scharffetter-Kochanek K (2015) Mesenchymal Stem Cells in Wound Repair, Tissue Homeostasis, and Aging. In: Geiger H, Jasper H, Florian MC (eds) Stem Cell Aging: Mechanisms, Consequences, Rejuvenation. Springer, Vienna Heidelberg New York, pp 287-318.
Jiang and Scharffetter-Kochanek (2020) Mesenchymal stem cells adaptively respond to environmental cues thereby improving granulation tissue formation and wound healing. Front Immunol. [submitted]
Qi Y, Jiang D, Sindrilaru A, Stegemann A, Schatz S, Treiber N, Rojewski M, Schrezenmeier H, Vander Beken S, Wlaschek M, Böhm M, Seitz A, Scholz N, Dürselen L, Brinckmann J, Ignatius A, Scharffetter-Kochanek K. (2014) TSG-6 Released from Intradermally Injected Mesenchymal Stem Cells Accelerates Wound Healing and Reduces Tissue Fibrosis in Murine Full-Thickness Skin Wounds. J Invest Dermatol. 134: 526-537.
Sindrilaru A, Peters T, Wieschalka S, Baican C, Baican A, Peter H, Hainzl H, Schatz S, Qi Y, Schlecht A, Weiss JM, Wlaschek M, Sunderkoetter C, Scharffetter-Kochanek K. (2011) An unrestrained inflammatory M1 macrophage population induced by iron impairs wound healing in humans and mice. J Clin Invest. 121:985-997.
Sindrilaru A and Scharffetter-Kochanek K (2013) Disclosure of the Culprits: Macrophages -Versatile Regulators of Wound Healing. Adv Wound Care 2: 357-368.
Wlaschek M and Scharffetter-Kochanek K (2005) Oxidative stress in chronic venous leg ulcers. Wound Rep Reg. 13: 452-461.
Wlaschek M, Singh K, Sindrilaru A, Crisan D, Scharffetter-Kochanek K. (2019) Iron and iron-dependent reactive oxygen species in the regulation of macrophages and fibroblasts in non-healing chronic wounds. Free Radic Biol Med. 133:262-275.
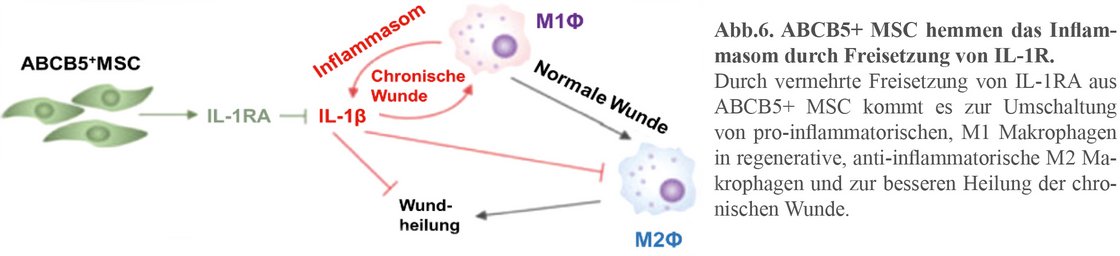
ABCB5+MSC beschleunigen die Heilung von chronisch venösen Ulzera
Wenn ABCB5+ MSC in chronisch Eisen-überladene Wunden transplantiert werden, kommt es zu einer beschleunigten Wundheilung dieser chronischen Wunden (Vander Beken et al., 2019). ABCB5+ MSC setzen präferentiell Interleukin-1 Rezeptor Antagonist (IL-1RA) frei, der die Bindung von IL-1β verhindert, und damit das aktivierte Inflammasom inhibiert. Deshalb kommt es auch zum Switch von pro-inflammtorischen M1 Makrophagen zu regenerativen, anti-inflammatorischen M2 Makrophagen im Ulkus. Das führt zur Abheilung der Entzündung und über die Freisetzung von Wachstumsfaktoren aus den M2 Makrophagen zur Ausbildung eines Granulations- und Ersatzgewebes. Das bedeutet, dass ABCB5+ MSC in der Lage sind, die Blockade des chronisch venösen Ulkus in der Entzündungsphase zu überwinden und die Wunde zur Abheilung zu bringen.
ABCB5+MSCs als „Adaptive Drug Stores“ – Studien zum klinischen Einsatz
Humane dermale ABCB5+ MSCs stellen nach diesen Untersuchungen eine vielversprechende Therapiemöglichkeit auch des chronisch venösen Ulkus des Menschen dar. Die ABCB5+ MSC wurden zunächst nach GLP-Richtlinien untersucht und für den GMP-konformen Einsatz als Medizinprodukte entsprechend der Richtlinien entwickelt (Tappenbeck et al., 2019). Erste Studien zum therapeutischen Einsatz wurden von TICEBA und RHEACELL multizentrisch initiiert (EudraCT Number: 2015-000399-81, 2017-000233-31, 000234-57) und weisen beim chronisch venösen Ulkus aber auch beim diabetischen Ulkus sehr gute Abheilungsraten auf. Diese müssen in größeren Studien bestätigt werden.
Es sollen langfristig unterschiedlich „geprimte“ MSCs für die Heilung von infizierten Wunden entwickelt werden.
Tappenbeck N, Schröder HM, Niebergall-Roth E, Hassinger F, Dehio U, Dieter K, Kraft K, Kerstan A, Esterlechner J, Frank NY, Scharffetter-Kochanek K, Murphy GF, Orgill DP, Beck J, Frank MH, Ganss C, Kluth MA. (2019) In vivo safety profile and biodistribution of GMP-manufactured human skin-derived ABCB5-positive mesenchymal stromal cells for use in clinical trials. Cytotherapy. S1465-3249.
DIE SUCHE NACH URSÄCHLICHEN, NEUEN GENEN ALS ZIELSTRUKTUREN NEUER THERAPIEN BEI DER PSORIASIS
(Dr. Rajeev Pandey, Dr. Kamayami Singh, Prof. Honglin Wang)
Wir haben zusammen mit Prof. Beaudet und seinem Team (Baylor College of Medicine in Houston, Texas) das hypomorphe (CD18hypo) PL/J-Mausmodell generiert. Diese Mäuse weisen eine verminderte Expression der gemeinsamen Kette von β2-Integrinen (CD11/CD18) auf, und entwickeln spontan eine T-Zell-vermittelte psoriasiforme Hauterkrankung. Dieses Psoriasis-Maus-Modell ähnelt klinisch und histologisch stark der menschlichen Psoriasis in seiner T-Zell-abhängigen Pathogenese, seiner polygenen Basis und seinem Ansprechen auf die Therapie. Depletierende Antikörper gegen CD4+, aber nicht gegen CD8+-T-Zellen, führten zur vollständigen Auflösung dieser psoriasiformen Hauterkrankung. CD18 stellt die gemeinsame β2-Kette der β2-Integrinfamilie dar, wobei 4 heterodimere Moleküle (CD11a/CD18, CD11b/CD18, CD11c/CD18 und CD11d/CD18) ausschließlich auf hämatopoetischen Zellen exprimiert werden. Neben weiteren Möglichkeiten kann eine verringerte CD18-Expression eine gestörte Bildung der immunologischen Synapse verursachen, was zur Erzeugung und Persistenz von autoreaktiven T-Zellen führt. So konnten wir zeigen, dass die verminderte Expression von CD18 zu einer vermehrten Bildung von Th17 Zellen auf Kosten von regulatorischen T-Zellen führt. Dieses Mausmodell erlaubt es mit genetischen Methoden die polygene Natur dieser Erkrankung aufzuklären, insbesondere von Genen, die für den psoriasiformen Phänotyp, neben der verminderten CD18 Expression, mitverantwortlich sind.
Fragen: Welche Gene sind für den psoriasiformen Genotyp mitverantwortlich? Die pathogene Rolle von β2-Integrinen bei menschlicher Psoriasis und anderen entzündlichen Hauterkrankungen ist wenig verstanden.
Singh K, Gatzka M, Peters T, Borkner L, Hainzl A, Wang H, Sindrilaru A, Scharffetter-Kochanek K. (2013) Reduced CD18 levels drive Treg conversion into Th17 cells in the CD18hypo PL/J mouse model of psoriasis. J Immunol. 190:2544-53.
Gatzka M, Hainzl A, Peters T, Singh K, Tasdogan A, Wlaschek M, Scharffetter-Kochanek K. (2013) Reduction of CD18 promotes expansion of inflammatory γδ T cells collaborating with CD4+ T cells in chronic murine psoriasiform dermatitis. J Immunol. 191:5477-88.
Wang H, von Rohrscheidt J, Roehrbein J, Peters T, Sindrilaru A, Kess D, Preissner KT, Scharffetter-Kochanek K. (2010) Extracellular adherence protein of Staphylococcus aureus suppresses diesease by inhibiting T-cell recruitment in a mouse model of psoriasis. J Invest Dermatol. 130:743-54.
Oreshkova T, Wang H, Seier A, Sindrilaru A, Varga G, Grabbe S, Scharffetter-Kochanek K, Peters T. (2009) Beta2 integrin-deficiency yields unconventional double-negative T cells distinct from mature classical natural killer cells in mice. Immunology. 128: 271-286.
Wang H, Peters T, Sindrilaru A, Scharffetter-Kochanek K. (2009) Key Role of Macrophages in the Pathogenesis of CD18 Hypomorphic Murine Model of Psoriasis. J Invest Dermatol. 129:1100-14.
Wang H, Syrovets T, Kess D, Buchele B, Hainzl H, Lunov O, Weiss JM, Scharffetter-Kochanek K, Simmet T. (2009) Targeting NFkappaB with a natural triterpenoid alleviates skin inflammation in a mouse model of psoriasis. J Immunol. 183:4755-4763.
Wang H, Kess D, Lindqvist A-KB, Peters T, Sindrilaru A, Wlaschek M, Blakytny R, Holmdahl R, Scharffetter-Kochanek K. (2008) A 9-cM interval of chromosome 10 controls the T-cell-dependent psoriasiform skin disease and arthritis in a murine psoriasis model. J Immunol. 180:5520-5529.
Wang H, Peters T, Sindrilaru A, Kess D, Oreshkova T, Yu X-Z, Seier AM, Schreiber H, Wlaschek M, Blakytny R, Röhrbein J, Schulz G, Weiss JM, Scharffetter-Kochanek K. (2008) TGF-β-dependent suppressive function of regulatory T-cells requires CD18 wild-type levels in a psoriasis murine model. J Clin Invest. 118:2629-2639.
Wang H, Peters T, Kess D, Sindrilaru A, Oreshkova T, Van Rooijen N, Stratis A, Sunderkoetter C, Wlaschek M, Haase I, Scharffetter-Kochanek K. (2006) Activated macrophages play an essential role in a T cell-dependent murine psoriasis model. J Clin Invest. 116:2105-2114.
Kess D, Lindqvist AKB, Peters T, Zamek J, Wang H, Nischt R, Broman KW, Blakytny R, Krieg T, Holmdahl R, Scharffetter-Kochanek K. (2006) Identification of susceptibility loci for the psoriasiform skin disease in a murine psoriasis model. J Immunol. 177:4612-9.
Kess D, Peters T, Zamek J, Wickenhauser C, Tawadros S, Loser K, Varga G, Grabbe S, Nischt R, Sunderkötter C, Müller W, Krieg T, Scharffetter-Kochanek K. (2003) CD4+ T cell associated pathophysiology critically depends on CD18 gene dose effects in a murine model of psoriasis. J Immunol. 171: 5697-5706.
Bullard DC*, Scharffetter-Kochanek K*, McArthur MJ, Chosay JG, McBride ME, Montgomery CA, Beaudet AL (1996) A polygenic mouse model of psoriasiform skin disease in CD18-deficient mice. Proc Natl Acad Sci U S A. 93(5):2116-21.
Drittmittel-geförderte Projekte
Deutsche Forschungsgemeinschaft (SFB1149 Trauma, GRK1789 CEMMA, Sachbeihilfe Einzelantrag), BMBF, Europäische Union, Exzellenz-Initiative International Graduate School Ulm/IGradU, Industriekooperationen, Landesstiftung Baden-Württemberg.
Medizinische Doktorarbeiten
Wir vergeben experimentelle Doktorarbeiten, die sich an Fragestellungen in den dargestellten Forschungsschwerpunkten orientieren. Ein Stipendium wird mit der Kandidatin/dem Kandidaten beantragt. Enge Betreuung im Seminar und außerhalb. Die Ausbildung in modernen Techniken an der zu bearbeiteten Fragestellung und Vermittlung allgemeiner Konzepte der Medizin wird angestrebt. Ein ganztägiger Einsatz ist für 12 Monate erforderlich.
Naturwissenschaftliche Doktorarbeiten
Wir vergeben experimentelle Doktorarbeiten, die sich an Fragestellungen in den dargestellten Forschungsschwerpunkten orientieren. Die Kandidaten können entweder einen Dr. biol. hum. der Medizinischen Fakultät oder, in Abhängigkeit von der Qualifikation, einen PhD oder Dr. rer. nat. im Rahmen der International Graduate School Ulm anstreben.
Kontakt Prof. Scharffetter-Kochanek
Telefon 0731-50057501 (Sekretariat)
Kontakt Dr. Wlaschek, Laborleiter
Telefon 0731-50057592
Arbeitsgruppe Professor Dr. med. Johannes Weiss
Immundermatologie
Die Arbeitsgruppe von Prof. Weiss hat sich über Jahre mit der Rolle von dendritischen Zellen im Rahmen von allergischen Hautreaktionen und entzündlichen Erkrankungen der Haut befasst. In den letzten Jahren lag hier ein besonderer Schwerpunkt auf der Rolle von Osteopontin (OPN), einem Protein mit diversen Funktionen, das im Immunsystem Zytokin-Funktionen ausübt und von verschiedenen Immunzellen sezerniert wird. Zuletzt wurde die Rolle von Osteopontin insbesondere im Rahmen des chronischen allergischen Kontaktekzems untersucht. Hierbei wurde gezeigt, dass das Retinoid 9-cis-Retinsäure (9cisRA), das auch zur Therapie von Handekzemen verwendet wird, die Ausdifferenzierung eines besonderen regulatorischen dendritischen Zellphänotyps induziert. Dendritische Zellen, die mit 9cisRA behandelt werden, exprimieren geringere Mengen des MHC-2-Komplexes und co-stimulatorischer Moleküle, aber verstärkt den inhibitorischen Co-Rezeptor PDA-1-Ligand. 9cisRA behandelte dendritische Zellen exprimieren weniger pro-inflammatorische Zytokine, exprimieren aber sehr viel Osteopontin und induzieen regulatorische T-Zellen (Treg). Das von dendritischen Zellen sezernierte Osteopontin ist für die Treg Differenzierung offensichtlich von besonderer Bedeutung, da OPN-defiziente dendritische Zellen schlechter Tregs induzieren können.
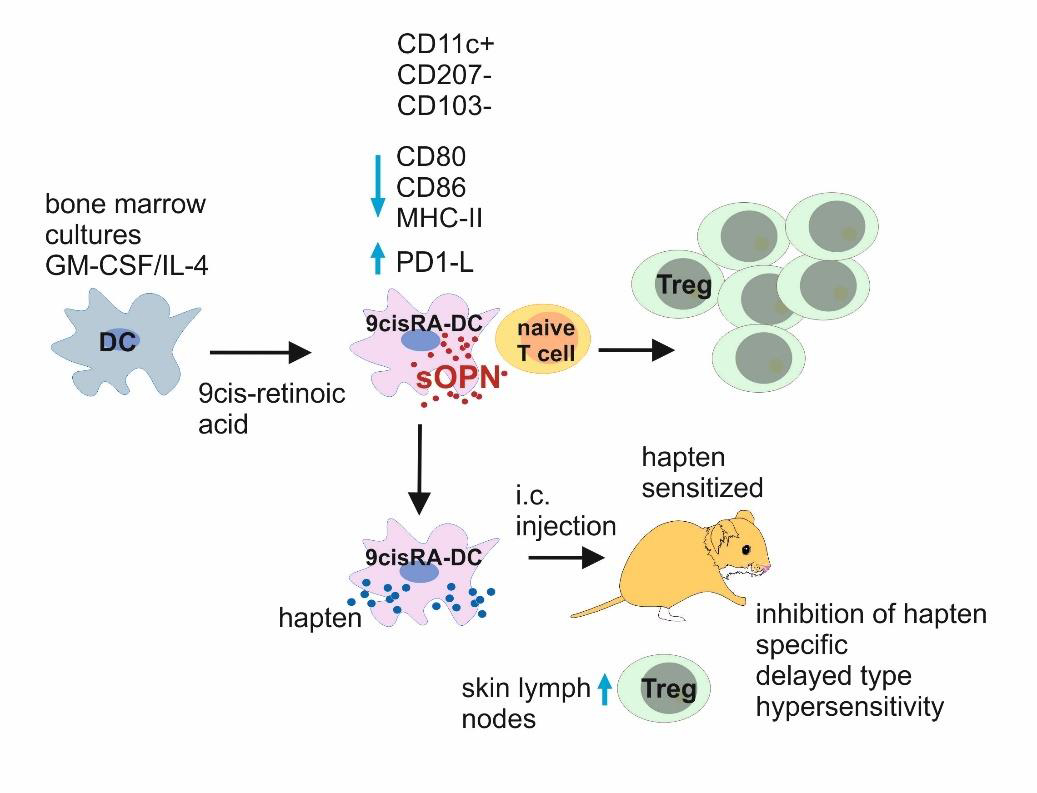
Key Messages
The pan retinoid receptor agonist 9cisRA that is used to treat chronic hand eczema mediates its anti-inflammatory potential through the induction of Treg inducing dendritic cells (DC).
Osteopontin from DC is a central mediator in the induction of Tregs as 9cisRA treatment induced Treg expanding function is inhibited upon osteopontin deficiency of DC.
9cisRA treated DC may be a potent tool to mediate tolerance in so far not erasable contact allergy.
Weiterer Überblick über ORCID iD 0000-0002-4071-8792
- Weiss JM, Sleeman J, Renkl AC, Dittmar HC, Termeer CC, Taxis S, Howells N, Hofmann M, Köhler G, Schöpf E, Ponta H, Herrlich P, Simon JC. An essential role for CD44 variant isoforms in epidermal Langerhans cell and blood dendritic cell function. J Cell Biol 137:1137-1147 (1997)
- Weiss JM, Renkl AC, Maier CS, Kimmig M, Liaw L, Ahrens T, Kon S, Maeda M, Hotta H, Uede T and Simon JC. Osteopontin is involved in the initiation of cutaneous contact hypersensitivity by inducing Langerhans and dendritic cell migration to lymph nodes. J Exp Med 194:19-1229 (2001)
- Renkl C, Wussler J, Ahrens T, Thoma K, Kon S, Uede T, Martin SF, Simon JC, Weiss JM. Osteopontin functionally activates dendritic cells and induces their differentiation towards a Th-1 polarizing phenotype. Blood 106:946-55 (2005)
- Buback F, Renkl AC, Schulz G, Weiss JM. Osteopontin and the skin: multiple emerging roles in cutaneous biology and pathology. Exp Dermatol 18:750-9 (2009)
- Seier AM, Renkl AC, Schulz G, Uebele T, Sindrilaru A, Iben S, Liaw L, Kon S, Uede T, Weiss JM. Antigen-specific induction of osteopontin contributes to the chronification of allergic contact dermatitis. Am J Pathol 176:246-258 (2010)
- Scheurmann J, Treiber N, Weber C, Renkl AC, Frenzel D, Buback F, Rueß A, Schulz G, Scharffetter-Kochanek K and Weiss JM. Mice with heterozygous deficiency of manganese superoxide dismutase (SOD2) have a skin immune system with features of “inflamm-aging”. Arch Dermatol Res 306:143-155 (2014)
- Frenzel D, Borkner L, Scheurmann J, Singh K, Scharffetter-Kochanek K and Weiss JM. Osteopontin deficiency affects imiquimod-induced psoriasis-like murine skin-inflammation and lymphocyte distribution in skin, draining lymph nodes and spleen. Exp Dermatol 24:305-7 (2015)
- Frenzel DF, Weiss JM. Osteopontin and allergic disease: pathophysiology and implications for diagnostics and therapy. Expert Rev Clin Immunol 7:93-109 (2011)
- Kraus LF, Scheurmann J, Frenzel D and Weiss JM. 9-cis-Retinoic Acid Induces a Distinct Regulatory Dendritic Cell Phenotype That Modulates Murine Delayed-Type Allergy. Contact Dermatitis 78:41-54 (2018)
- Weiss JM. Osteopontin regulatory functions in the hair follicle open a therapeutic approach for hypertrichosis.Br J Dermatol 182:1324-1325 (2020)
Forschungsprojekt „Die IL-17/Osteopontin-Achse bei Psoriasis: Krankheitsverlauf und Komorbiditäten“
Ziel des Projekts ist die Bestimmung von Plasma-Zytokinen, insbesondere auch OPN- und Th17-Zytokinen im Serum von Psoriasispatienten im Rahmen der klinischen Routine unter Psoriasis Therapie. Die Erhebung erfolgt im Rahmen der Psoriasissprechstunde an der Universitätsklinik für Dermatologie und Allergologie.
Abstract aus dem Projekt bei FoBi-Digital 2020
Die Modulation der IL-17/Osteopontin-Achse bei Psoriasis im Krankheitsverlauf und bei Komorbiditäten unter „Real-Life“-Bedingungen
Julian Schmid, Lea F. Kraus und Johannes M. Weiss
Universitätsklinik für Dermatologie und Allergologie Ulm
Osteopontin (OPN) besitzt pro- und anti-inflammatorische Zytokinwirkungen. Bei multipler Sklerose induziert OPN aus Dendritischen Zellen die Produktion von IL-17 in CD4+ T-Zellen und perpetuiert die Entzündung. Hohe OPN-Spiegel wurden bei Psoriasispatienten mit Komorbiditäten assoziiert. Ziel des Projektes war es, unter den „Real-Life“-Bedingungen einer Psoriasissprechstunde an vorhandenen Routineproben den Einfluss der Therapie auf die OPN-Plasmaspiegel bei Psoriasispatienten zu untersuchen, diese in den Gesamtkontext der Zytokinregulation zu stellen sowie die Zytokinmuster mit dem Erkrankungsverlauf und Komorbiditäten zu korrelieren.
An der Universitätsklinik für Dermatologie Ulm wurden anhand einer Serum-/Plasmaproben-Bank die Daten von 148 konsekutiv vorstelligen Psoriasispatienten zu zwei Therapiezeitpunkten (T1 und T2) ausgewertet. Die Therapiemodalitäten reichten von Lokaltherapie bis zu Biologika. Daten von 118 Patienten (73 Männer und 45 Frauen, Durchschnittsalter 53 Jahre) konnten ausgewertet werden. Im Serum/Plasma wurden IL-12, IL-17, IL-23, IFNγ, TNFα, IL-4, IL-10 und OPN bestimmt.
Für IL-4, IL-10, IL-12 und IL-17 fanden sich nur geringe Konzentrationen, höhere für IL-23, IFNγ und TNFα. Zugleich war OPN im Plasma stark erhöht. Zwischen Zeitpunkt T1 und T2 kam es tendenziell zu einem Abfall der mittleren Zytokinkonzentration von IL-4, IL-10, IL-17, IL-23 und OPN, wohingegen IL-12, TNFα und IFNγ leicht anstiegen. Die OPN-Konzentration korrelierte negativ mit dem Th2-Zytokin IL-4 und positiv mit anti-inflammatorischem IL-10 (T2). Die Auswertung von Patienten mit gutem Therapieansprechen (ΔPASI ≤ -5) zeigte einen signifikanten Anstieg des IL-10 und IL-4 sowie Reduktion von IFNγ, nicht aber von OPN.
Bezüglich Komorbiditäten fand sich bei Patienten mit Bluthochdruck (T1) und bei schwerer Psoriasis > 10 Jahren eine signifikant höhere OPN-Konzentration. Körperlich inaktive Patienten, Diabetiker (T2) und Patienten mit Psoriasisarthritis (T1) hatten eine höhere IL-12 Konzentration, Nikotin konsumierende höheres IL-23.
Zusammenfassend deutet diese Studie darauf hin, dass bei bestimmten Komorbiditäten die pro-inflammatorischen Zytokine erhöht sind. Es bestätigt sich, dass OPN bei Psoriasis in hohen Konzentrationen nachweisbar ist. Eine signifikante Modulation von OPN unter Therapie ließ sich nicht nachweisen.
Mitarbeiter des Projekts:
Julian Schmid
Dr. med. Lea Kraus
Das Projekt wurde anteilig durch die Novartis Pharma GmbH unterstützt.
Versorgungsforschung
Forschungsprojekt „Psoriasis Arthritis und Komorbiditäten bei Psoriasis: Ein Interdisziplinäres Projekt zur Versorgungsforschung“
Es handelt sich um ein Projekt, bei dem anhand eines Patientenfragebogens die Versorgungssituation bezüglich Psoriasis Arthritis und Psoriasis-Komorbiditäten im Raum Ulm erhoben werden soll. Die Daten werden erhoben im Rahmen einer interdisziplinären Psoriasissprechstunde. Partner des Projekts ist die Rheumatologische Abteilung am Alb-Donau Klinikum Langenau, Dr. med. Steffen Briem.
Doktoranden im Projekt:
Frau S. Thiess
Frau C. Eckert
Frau S. Prox-Ambil
Das Projekt wird anteilig durch die Novartis Pharma GmbH unterstützt.
Allergologische Forschung
NSAID Intoleranz
Retrospektive Betrachtung von Patienten mit Analgetika-Hypersensitivität
Zusammenfassung Dissertation Dr. med. Martin Winter
NSAR (Nichtsteroidale Antirheumatika) gehören zu den am häufigsten verordneten Medikamenten und sind nach Antibiotika der zweithäufigste vermutete Auslöser für eine Arzneimittelhypersensitivität. Aufgrund verschiedener Pathomechanismen ist das auslösende Agens häufig weder eindeutig zu identifizieren, noch eine Garantie dafür, dass andere NSAR sicher eingenommen werden können. Der Goldstandard zur Diagnostik einer Medikamentenunverträglichkeit ist die Medikamentenprovokationstestung.
Ziel der Arbeit war es, Zusammenhänge zwischen einer nachgewiesenen Analgetikaintoleranz, Schwere der klinischen Reaktion während der Provokationstestung, einer erhöhten Mastzelltryptase im Serum, Relevanz der Hauttestungen zur Diagnostik einer Analgetika-Hypersensitivität, höherem Lebensalter sowie Verträglichkeit anderer COX-Inhibitoren (Cyclooxygenase-Inhibitoren) (insbesondere COX-2-Inhibitoren) zu analysieren. Hierfür wurden 438 Patienten aus den Jahren 2004 bis 2014 untersucht, die in der Klinik für Dermatologie und Allergologie der Universität Ulm eine Medikamentenprovokation erhalten haben. Die Auswertung ergab, dass ein höheres Lebensalter (> 60 Jahre) nicht mit einer erhöhten Prävalenz für eine Analgetikaintoleranz einhergeht. Eindeutige Risikofaktoren, die auf eine erhöhte Prävalenz hinweisen, konnten weder im Alter noch in der Geschlechterverteilung gesehen werden.
Eine erhöhte Mastzelltryptase ist ein Indikator für eine systemische Mastozytose und damit einhergehend für ein höheres Risiko für schwere anaphylaktische Reaktionen. In der Studienpopulation entsprach die Prävalenz für eine erhöhte Mastzelltryptase zwar der Normalbevölkerung, jedoch hatte nur ein Patient in der Gruppe der nachgewiesenen Medikamentenunverträglichkeit eine erhöhte Mastzelltryptase. Im Vergleich zu den übrigen Studienpatienten ist die erhöhte Mastzelltryptase jedoch kein Risikofaktor für eine häufigere oder schwerere anaphylaktische Reaktion in der Medikamentenprovokationstestung.
COX-2-Inhibitoren werden von 96 % aller Patienten mit nachgewiesener NSAR-Hypersensitivität vertragen. Vereinzelt liegen sowohl Typ-I- als auch Typ-IV-Sensibilisierungen gegenüber einem COX-2-Inhibitor (Celecoxib) vor, jedoch hat nur ein Patient auf einen anderen (überwiegenden) COX-2-Inhibitor (Nimesulid) reagiert. Dennoch zeigt die Arbeit, dass COX-2-Inhibitoren mit hoher Wahrscheinlichkeit vertragen werden, wenn eine Unverträglichkeit gegenüber einem COX-1-Inhibitor vorliegt. Die erste Einnahme sollte dennoch unter ärztlicher Aufsicht und Notfallbereitschaft erfolgen.
Zusammenfassend zeigt diese retrospektive Studie, dass bei 438 Patienten, die in den Jahren 2004 bis 2014 in der Klinik für Dermatologie und Allergologie der Universitätsklinik Ulm eine Medikamentenprovokation erhalten haben, ein höheres Lebensalter (> 60 Jahre) nicht mit einer erhöhten Prävalenz für eine Analgetikaintoleranz einhergeht. Auch ist eine erhöhte Mastzelltryptase (≥ 11,4 μg) bei Patienten, die eine NSAR-Provokationstestung erhalten, kein Risikofaktor für eine schwere anaphylaktische Reaktion. Zudem wurden COX-2-Inhibitoren von 96 % aller Patienten mit nachgewiesener NSAR-Hypersensitivität vertragen. Demnach wurden fast alle COX-2-Inhibitoren auch bei Vorliegen einer Unverträglichkeit gegenüber einem COX-1-Inhibitor vertragen.
Link zur Dissertation: https://oparu.uni-ulm.de/xmlui/handle/123456789/8146
Mitarbeiter des Projekts:
Dr. med. Christian Martin Winter
Dissertationen aus Projekten der Arbeitsgruppe
Expression von Osteopontin im Rahmen der Entzündungsreaktion bei Psoriasis vulgaris, Susanne-Katharina Höppner, 2012 oparu.uni-ulm.de/xmlui/handle/123456789/2774
Insektengiftallergie: Vergleich von Kindern und Erwachsenen bezüglich diagnostischer Parameter und Verträglichkeit der spezifischen Immuntherapie an der Universitätsklinik für Dermatologie und Allergologie Ulm, Christina Schachtner, 2012 oparu.uni-ulm.de/xmlui/handle/123456789/2736
Die Expression von Osteopontin und seinen Rezeptoren bei allergischen Kontaktekzemen, Tanja Uebele, 2013 oparu.uni-ulm.de/xmlui/handle/123456789/3062
Die Rolle von Osteopontin für die Chronifizierung allergischer Kontaktekzeme, Anne Seier, 2008 (Dr. biol. hum.)
Die Rolle der Mangan-Superoxiddismutase für die Funktion von Dendritischen Zellen, Christine Weber, 2015
Einfluss von verschiedenen Portkatheter-Systemen auf die Flussraten bei der extrakorporalen Photopherese, Annerose Straub, (2016) oparu.uni-ulm.de/xmlui/handle/123456789/4027
Rekombinante Allergene in der Diagnostik der Hymenopterengift Allergie, Andreas Benedikt Weins, 2016
9-cis-retinoic acid modulates dendritic cell differentiation towards a regulatory T cell inducing phenotype, Lea-Franziska Kraus, 2018 oparu.uni-ulm.de/xmlui/handle/123456789/5503
Retrospektive Betrachtung von Patienten mit Analgetika-Hypersensitivität, Christian Martin Winter, oparu.uni-ulm.de/xmlui/handle/123456789/8146
Vergabe von Dissertations-Projekten
Es werden medizinische Dissertationen betreut. Um eine gute Betreuung gewährleisten zu können, werden zeitgleich nur wenige Arbeiten vergeben. Aktuell werden vor allem Arbeiten im Bereich der Versorgungsforschung und der klinischen allergologischen Forschung vergeben. Für die Durchführung einer Dissertation ist ein Freisemester erforderlich, während dem man sich in der vorlesungsfreien Zeit vor und nach dem Freisemester voll dem Projekt widmen kann.
Arbeitsgruppe Priv.-Doz. Dr. med. Sebastian Iben

PD Dr. Sebastian Iben

Fatima Khalid - PhD Student

Tamara Phan - PhD Student

MingYue Qiang - MD Student

Gaojie Zhu - MD Student

Maximilian Wagner - (Alumnus)

Adrian Schelling - Technischer Assistent

Sarah Müller - Masterstudentin
Vorzeitige Alterung verstehen um Alterungskrankheiten aufzuklären
(Fatima Khalid, Tamara Phan, MingYue Qiang, , Gaojie Zhu, Adrian Schelling, Maximilian Wagner, Sarah Müller) (Fatima Khalid, Tamara Phan, MingYue Qiang, , Gaojie Zhu, Adrian Schelling, Maximilian Wagner, Sarah Müller)
Die Haut und ihre Anhangsgebilde ist unser Indexorgan für die Einschätzung des Alters eines Menschen. Deswegen untersuchen wir in der Hautforschung die Mechanismen, die die Haut und den Organismus altern lassen. Krankheiten, bei denen genetische Defekte zu beschleunigter Alterung führen dienen uns als Model um diese Mechanismen aufzuklären. Das Cockayne Syndrom und die Trichothiodystrophie sind verwandte Krankheiten, bei denen Gendefekte zur Alterung im Zeitraffer führen. Schon im Kindesalter findet man Symptome des alternden Körpers bei diesen Patienten, mit Verlust des Unterhautfettgewebes, Haarausfall, Degeneration des zentralen Nervensystems und ausbleibendes Wachstum und Entwicklung. Hautzellen von diesen Patienten werden von uns untersucht um zu verstehen, welche zellulären Signalwege gestört sind. Dabei konzentrieren wir unsere Arbeiten auf die Untersuchung der Ribosomenbiogenese, da die Gendefekte, welche die Krankheiten auslösen, auch die Herstellung der Proteinfabriken, der Ribsomen, stören. Was sind die zellulären und organismalen Folgen einer gestörten Ribosomenbiogenese? Kann man das ausbleibende Wachstum und die Degeneration insbesondere des zentralen Nervensystems mit Fehlern in den Proteinfabriken erklären? Erste Ergebnisse unserer Arbeiten deuten in diese Richtung. Wir konnten zeigen, dass in Hautzellen von Cockayne Syndrom Patienten ein „Circulus vitiosus“, ein Teufelskreis, aktiv ist, der das Wachstum der Zellen unterdrückt. Die Arbeit der vergangenen Dekaden hatte gezeigt, dass alle Gene, deren Defekte das Cockayne Syndrom auslösen, auch eine Rolle bei der Ribosomenherstellung spielen. Wenn diese Synthese gestört ist, dann werden auch Ribosomen hergestellt, die fehleranfällig sind. Diese Ribosomen stellen fehlerhafte Proteine her, die die Zellen stressen und zu einer Antwort führen, die die Neusynthese von Ribosomen unterdrückt. Damit haben die Zellen zu wenige Proteinfabriken, und die Proteinfabriken, die hergestellt werden, arbeiten fehlerhaft. Dieser Teufelskreis kann, zumindest in der Zellkulturschale, durch die Gabe von Proteinfaltern, Chaperonen, durchbrochen werden. Die Unterdrückung der Ribsomenbiogenese und der Proteinsynthese wird aufgehoben.
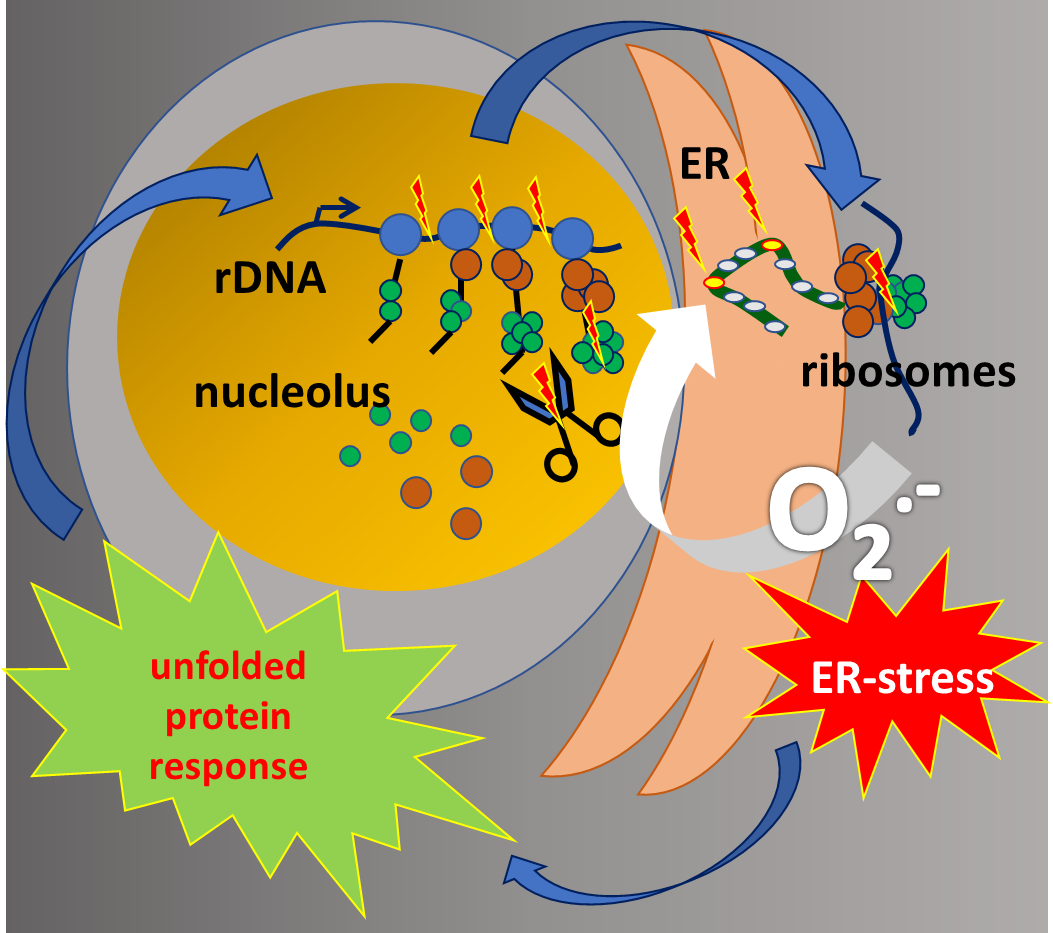
Zentrale Hypothese unserer Arbeiten: Die rRNA Transkription, der Schlüsselschritt der Ribosomenbiogenese, ist gestört und führt zu Ribsomen, die ihrerseits fehlerhafte Eiweiße herstellen. Als Reaktion wird die Bildung neuer Eiweiße unterdrückt, wie auch die Herstellung neuer Ribosomen.
Iben, S., Tschochner, H., Bier, M., Hoogstraten, D., Hozak, P., Egly, J.M. and Grummt, I. (2002) TFIIH plays an essential role in RNA polymerase I transcription. Cell,109, 297-306.
Bradsher, J., Auriol, J., Proietti de Santis, L., Iben, S., Vonesch, J.L., Grummt, I. and Egly, J.M. (2002) CSB is a 7. component of RNA pol I transcription. Mol Cell,10, 819-829.
Assfalg, R., Lebedev, A., Gonzalez, O.G., Schelling, A., Koch, S. and Iben, S. (2012) TFIIH is an elongation factor of RNA polymerase I. Nucleic Acids Res,40, 650-659.
Koch S, Garcia Gonzalez O, Assfalg R, Schelling A, Schäfer P, Scharffetter-Kochanek K, Iben S. (2014) Cockayne syndrome protein A is a transcription factor of RNA polymerase I and stimulates ribosomal biogenesis and growth.Cell Cycle. 13, 2029-37
Alupei MC, Maity P, Esser PR, Krikki I, Tuorto F, Parlato R, Penzo M, Schelling A, Laugel V, Montanaro L, Scharffetter-Kochanek K, Iben S. (2018) Loss of Proteostasis is a Pathomechanism in Cockayne Syndrome. Cell Rep.6 1612-1619
Cockayne Syndrom- welche Veränderungen in den Ribosomen führen zu einem Verlust des Proteingleichgewichtes?
(Dr.Marius Alupei (Alumnus), MingYue Qiang)
In Hautzellen von Cockayne Syndrom Patienten konnten wir eine fehlerhafte Proteinsynthese nachweisen (Alupei et al, 2018). Diese führt zu einem Verlust der Proteinhomöostase und deren zellulären Folgen. Nun untersuchen wir, welche Veränderungen an den Ribosomen zu der verschlechterten Qualität der Proteinsynthese führen. Es wird die Reifung der ribosomalen RNA untersucht, wie auch die Zusammensetzung der Ribosomen in massenspektrometrischen Analysen und Western Blots. Ungelöste Fragen: Ist die Zusammensetzung der Ribosomen in Cockayne Syndrom Patientenzellen verändert und könnten diese Veränderungen die Ungenauigkeit der Proteinsynthese erklären? Wird die Synthese der Ribosomen durch Gabe pharmazeutischer Chaperone wieder normalisiert? Zeigen auch die Mausmodelle des Cockayne Syndroms einen Verlust der Prozeinhomöostase und kann man diese durch Chaperongabe behandeln?
Bradsher, J., Auriol, J., Proietti de Santis, L., Iben, S., Vonesch, J.L., Grummt, I. and Egly, J.M. (2002) CSB is a component of RNA pol I transcription. Mol Cell,10, 819-829.
Lebedev, A., Scharffetter-Kochanek, K. and Iben, S. (2008) Truncated Cockayne syndrome B protein represses elongation by RNA polymerase I. J Mol Biol,382, 266-274.
Assfalg, R., Lebedev, A., Gonzalez, O.G., Schelling, A., Koch, S. and Iben, S. (2012) TFIIH is an elongation factor of RNA polymerase I. Nucleic Acids Res,40, 650-659.
Koch S, Garcia Gonzalez O, Assfalg R, Schelling A, Schäfer P, Scharffetter-Kochanek K, Iben S. (2014) Cockayne syndrome protein A is a transcription factor of RNA polymerase I and stimulates ribosomal biogenesis and growth.Cell Cycle. 13, 2029-37
Alupei MC, Maity P, Esser PR, Krikki I, Tuorto F, Parlato R, Penzo M, Schelling A, Laugel V, Montanaro L, Scharffetter-Kochanek K, Iben S. (2018) Loss of Proteostasis is a Pathomechanism in Cockayne Syndrome. Cell Rep.6 1612-1619
Trichothiodystrophie- gekennzeichnet durch einen Verlust der Proteinhomöostase?
(Fatima Khalid, Tamara Phan)
Die Trichothiodystrophie ist eine dem Cockayne Syndrom verwandte Krankheit, die neben Wachstumsstörungen und Zeichen vorzeitiger Alterung noch einen typischen Haut- und Haar Phänotyp aufweist. Die molekulare Ursache dieser Krankheit wird intensiv diskutiert und in diesen Projekten wird untersucht, ob defekte Ribosomen bei der Krankheitsentstehung beteiligt sind. Dazu untersuchen die beteiligten Mitarbeiter jeweils zwei Mutationen in unterschiedlichen Genen, die alle zu Trichothiodystrophie führen. Ungelöste Fragen: Finden wir in der Trichothiodystrophie die gleichen Krankheitsmechanismen wie im Cockayne Syndrom? Sind auch diese Zellen durch einen Verlust der Proteinhomöostase gekennzeichnet und kann diese durch Gabe von pharmazeutischen Chaperonen behandelt werden? Wirken diese Chaperone im Mausmodell der Trichothiodystrophie?
Störungen der Proteinsynthese am Ribosom als Grundlage neurodegenerativer Erkrankungen
(Maximilian Wagner (Alumnus), Sarah Müller)
Cockayne Syndrom und Trichothiodystrophie sind Modelerkrankungen anhand deren man grundsätzliche Mechanismen von Alterungserkrankungen verstehen möchte. In diesem Projekt überprüfen wir, ob die aus dem Studium der Voralterungserkrankungen gewonnenen Erkenntnisse auf typische Alterungserkrankungen anwendbar sind. Da neurologische Erkrankungen durch einen Verlust der Proteinhomöostase gekennzeichnet sind und Cockayne Syndrom und Trichothiodystrophiepatienten neurodegenerative Symptome zeigen, untersuchen wir, ob bei typischen neurodegenerativen Erkrankungen wie Huntington´s Erkrankung oder der Parkinson Demenz auch eine Beteiligung der Ribosomen nachweisbar ist. Wir wollen überprüfen, ob Erkenntnisse aus der Hautforschung allgemeine Gültigkeit haben. Ungelöste Fragen: Finden wir Störungen der Ribosomenbiogenese inneurodegenerativen Erkrankungen wie Huntington, Parkinson, Alzheimer und Amyotropher Lateralsklerose? Können diese Störungen den Verlust des Proteingleichgewichts erklären und führen diese Störungen zum Nervenzelluntergang?
Jesse S, Bayer H, Alupei MC, Zügel M, Mulaw M, Tuorto F, Malmsheimer S, Singh K, Steinacker J, Schumann U, Ludolph AC, Scharffetter-Kochanek K, Witting A, Weydt P, Iben S (2017) Ribosomal transcription is regulated by PGC-1alpha and disturbed in Huntington´s disease. Sci Rep. 2017 Aug 17;7(1):8513
Drittmittel geförderte Projekte
Unsere Arbeiten werden von der Deutschen Forschungsgemeinschaft DFG gefördert (Graduiertenkolleg 1789 CEMMA, Einzelantrag) wie auch vom Europäischen Huntington Disease Netzwerk EHDN).
