Das Team von Frau Prof. Friederike Liesche-Starnecker verbindet moderne Neuropathologie mit innovativen digitalen Analyseverfahren und translationaler Forschung.
Ein besonderer Schwerpunkt liegt hierbei auf der computergestützten (Neuro-)Pathologie. Durch die Kombination klassischer histopathologischer Diagnostik mit digitalen und KI-basierten Methoden eröffnen sich neue Möglichkeiten, komplexe Bilddaten objektiv und reproduzierbar auszuwerten.
Ein zentraler thematischer Fokus liegt bei der humanen Bornavirus-Enzephalitis, eine seltene, aber dafür bislang fast immer tödlichen und damit zunehmend relevanten zoonotischen Erkrankung. Ziel unserer Forschung ist es, die immunologischen und pathogenetischen Mechanismen dieser neurotropen Virusinfektion besser zu verstehen. Dabei untersuchen wir insbesondere Prozesse der Virusausbreitung, der Wirt-Virus-Interaktion sowie immunvermittelte Schädigungen des Nervensystems.
Darüber hinaus engagiert sich das Team im Bereich der translationalen Neuroonkologie. Hier stehen die biologischen Grundlagen aggressiver Hirntumoren, ihre Interaktion mit der Tumorumgebung sowie die Aufschlüsselung der Tumorheterogenität im Vordergrund. Durch die enge Verbindung von Forschung und klinischer Anwendung möchten wir dazu beitragen, innovative Erkenntnisse schneller in die Versorgung von Patientinnen und Patienten zu überführen.
Auf dieser Seite finden Sie weitere Informationen zu unseren Forschungsschwerpunkten und aktuellen Projekten. Wir freuen uns jederzeit über den Austausch mit interessierten Partnerinnen und Partnern sowie über neue wissenschaftliche Kooperationen. Auch Anfragen zur Mitarbeit im Rahmen von Abschlussarbeiten oder Promotionen sind herzlich willkommen.
Forschungsschwerpunkte
Immunologie und Pathogenese bei der humanen Bornavirus-Enzephalitis
Das Borna disease virus 1 (BoDV-1) ist ein seltenes neurotropes Virus, das beim Menschen schwere und häufig tödlich verlaufende Gehirnhautentzündungen auslösen kann. Lange Zeit war es nur aus der Tiermedizin bekannt, insbesondere bei Pferden und Schafen. Erst seit 2018 ist belegt, dass BoDV-1 auch Menschen betrifft. Das Virus kommt vor allem in Bayern vor und gilt bisher als nicht behandelbar.
Die Arbeitsgruppe beschäftigt sich seit mehreren Jahren mit der Erforschung des Bornavirus, mit einem Schwerpunkt auf der immunologischen und pathogenetischen Charakterisierung von Borna disease virus 1 (BoDV-1). Ziel ist es, grundlegende Mechanismen des Viruseintritts, der Ausbreitung im Nervensystem und der Interaktion mit der Wirtsimmunantwort zu verstehen. VSBV-1, ein weiteres zoonotisches Bornavirus mit humaner Pathogenität, wird dabei vergleichend untersucht.
Ein zentraler Fokus liegt auf der Immunpathologie der humanen Bornavirus-Enzephalitis, insbesondere im Vergleich zur tierischen Infektion sowie auf der Charakterisierung von Mikroglia und ZNS-assoziierten Makrophagen. Mithilfe räumlich aufgelöster transkriptomischer, proteomischer und bildgebender Verfahren werden virusinfizierte Zellen, lokale Immunantworten und Disseminationswege von BoDV-1 im zentralen und peripheren Nervensystem analysiert.
Aufgrund ihres Modellcharakters liefern diese Arbeiten grundlegende Erkenntnisse zu neurotropen Virusinfektionen und zu immunvermittelten Erkrankungen des Nervensystems.
ZooBoFo Bavaria 2.0 – Bornavirus im One-Health-Kontext
Im Projekt „Zoonotic Bornavirus Focalpoint Bavaria 2.0“ (ZooBoFo Bavaria 2.0) verfolgen wir einen konsequenten One-Health-Ansatz, um Übertragungswege des Virus besser zu verstehen und Präventionsstrategien weiterzuentwickeln. Das Projekt bündelt interdisziplinäre Expertise aus Human- und Veterinärmedizin, Umweltforschung und Neuropathologie. Zentrale Bausteine sind unter anderem Reservoirstudien in Spitzmäusen, autopsiebasierte klinische Forschung sowie die Weiterentwicklung diagnostischer und antiviraler Ansätze.
ZooBoFo Bavaria 2.0 wird vom Bayerischen Landesamt für Gesundheit und Lebensmittelsicherheit (LGL) koordiniert und entsteht in enger Kooperation mit dem Universitätsklinikum Regensburg, dem Friedrich-Loeffler-Institut (FLI) und weiteren Partnern. Das Vorhaben wird durch das Bayerische Staatsministerium für Gesundheit, Pflege und Prävention gefördert.
INSIGHT – Mikroglia und Immunreaktionen bei Bornavirus-Enzephalitis
Im Projekt INSIGHT (Investigating Microglia Signatures in Human Tissue) untersuchen wir, wie das hirneigene Immunsystem, insbesondere Mikroglia und ZNS-assoziierte Makrophagen, auf eine Bornavirus-Infektion reagiert. Ziel ist es, krankheitsspezifische Immunzell-Signaturen im menschlichen Gewebe zu identifizieren und neue Einblicke in die Pathogenese neurotropischer Virusinfektionen zu gewinnen.
INSIGHT entsteht in enger Kooperation mit Dr. Jana Koch aus der Arbeitsgruppe für Zelluläre Neuroanatomie am Lehrstuhl für Anatomie und Zellbiologie der Universität Augsburg (Prof. Dr. Peter Wieghofer), die über besondere Expertise in der Mikroglia- und Makrophagenbiologie verfügt.
Jungbäck N, Grochowski P, Hieber D, Dinser M, Mielewczyk Z, Pfefferkorn T, Muntau B, Richter T, Rieder G, Bayas A, Hirschbühl K, Märkl B, Adam P, Tappe D, Liesche-Starnecker F. Multimodal profiling of immune responses reveals innate-adaptive immune imbalance in human bornavirus encephalitis. Acta Neuropathol Commun 14, 109 (2026). doi: 10.1186/s40478-026-02319-6.
Michelakaki E, Schade B, Boehm B, Kappe E, Suchowski M, Kupca A, Schumacher M, Gager AM, Liesche-Starnecker F, Fiedler S, Schwarz E, Bago Z, Blutke A, Beer M, Rubbenstroth D, Matiasek K. Borna disease virus 1 as cause of fatal meningoencephalomyelitis in wild hedgehogs, Germany, 2022–2025. Emerg Infect Dis (2026). doi: 10.3201/eid3205.250952.
Vollmuth Y, Jungbäck N, Grochowski P, Mögele T, Stark L, Zarrabi NS, Schlegel J, Schaller T, Märkl B, Matiasek K, Liesche-Starnecker F. Mapping Bornavirus encephalitis-A comparative study of viral spread and immune response in human and animal dead-end hosts. PLoS Pathog 21, 8 (2025). doi: 10.1371/journal.ppat.1013400. PMID: 40758738. PMCID: PMC12338802.
Jungbäck N, Vollmuth Y, Mögele T, Grochowski P, Schlegel J, Schaller T, Märkl B, Herden C, Matiasek K, Tappe D, Liesche-Starnecker F. Neuropathology, pathomechanism, and transmission in zoonotic Borna disease virus 1 infection: a systematic review. Lancet Infect Dis. 25, 4 (2025). doi: 10.1016/S1473-3099(24)00675-3. PMID: 39793593.
Ebinger A, Santos PD, Pfaff F, Dürrwald R, Kolodziejek J, Schlottau K, Ruf V, Liesche-Starnecker F, Ensser A, Korn K, Ulrich R, Fürstenau J, Matiasek K, Hansmann F, Seuberlich T, Nobach D, Müller M, Neubauer-Juric A, Suchowski M, Bauswein M, Niller HH, Schmidt B, Tappe D, Cadar D, Homeier-Bachmann T, Haring VC, Pörtner K, Frank C, Mundhenk L, Hoffmann B, Herms J, Baumgärtner W, Nowotny N, Schlegel J, Ulrich RG, Beer M, Rubbenstroth D. Lethal Borna disease virus 1 infections of humans and animals - in-depth molecular epidemiology and phylogeography. Nat Commun. 15, 7908 (2024). doi: 10.1038/s41467-024-52192-x. PMID: 39256401. PMCID: PMC11387626.
Bayas A, Menacher M, Lapa C, Tappe D, Maurer C, Liesche-Starnecker F, Schneider H, Naumann M. 18fluorodeoxyglucose PET/CT as possible early diagnostic tool preceding MRI changes in Borna disease virus 1 encephalitis. Lancet. 403, 10427 (2024). doi: 10.1016/S0140-6736(24)00049-7. PMID: 38368015.
Vollmuth Y, Jungbäck N, Mögele T, Schmidt-Graf F, Wunderlich S, Schimmel M, Rothe C, Stark L, Schlegel J, Rieder G, Richter T, Schaller T, Tappe D, Märkl B, Matiasek K, Liesche-Starnecker F. Comparative study of virus and lymphocyte distribution with clinical data suggests early high dose immunosuppression as potential key factor for the therapy of patients with BoDV-1 infection. Emerg Microbes & Infections 13 (2024). doi: 10.1080/22221751.2024.2350168; PMID: 38687703. PMCID: PMC11107860.
Liesche-Starnecker F, Schifferer M, Schlegel J, Vollmuth Y, Rubbenstroth D, Delbridge C, Gempt J, Lorenzl S, Schnurbus L, Misgeld T, Rosati M, Beer M, Matiasek K, Wunderlich S, Finck T. Hemorrhagic lesion with detection of infected endothelial cells in human bornavirus encephalitis. Acta Neuropathol. 144, 2 (2022). doi: 10.1007/s00401-022-02442-3. PMID: 35657496. PMCID: PMC9164175.
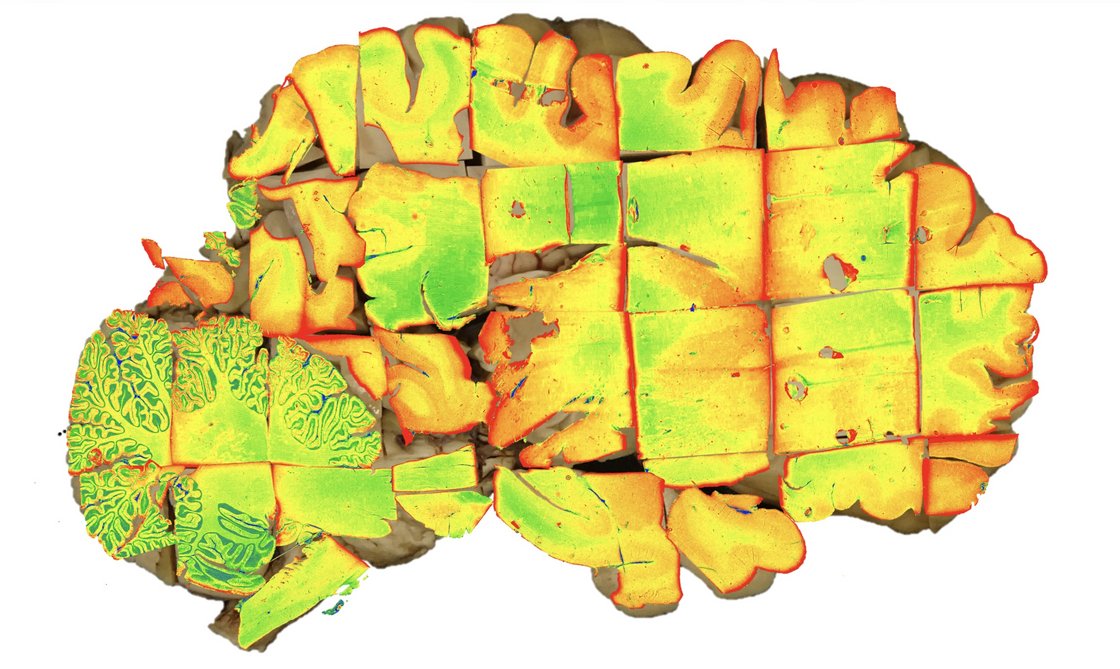
Angewandte Informatik für die medizinische Forschung
Die computergestützte Neuropathologie beschäftigt sich mit der Entwicklung und Anwendung informationstechnischer Methoden zur Analyse neuropathologischer Daten. Im Vordergrund des Forschungsschwerpunkts steht dabei die Unterstützung der anderen Forschungsschwerpunkte durch die systematische und automatisierte Auswertung der umfangreichen Datensätze. So können diagnostische, pathogenetische und translationale Fragestellungen effizient und reproduzierbar bearbeitet werden.
Im Methodikfokus steht momentan die automatisierte und interaktive Auswertung digitaler histologischer Präparate (Whole Slide Imaging). Hierfür werden Verfahren aus der Bildverarbeitung, dem maschinellen Lernen und der künstlichen Intelligenz eingesetzt, um Gewebestrukturen zu segmentieren, Zellpopulationen zu charakterisieren und krankheitsspezifische Muster zu identifizieren.
Künftige Projekte sollen den Fokus auf die Integration multimodaler Daten erweitern. Histologische Befunde werden so mit molekularen, transkriptomischen und klinischen Informationen verknüpft, um komplexe Krankheitsmechanismen besser zu verstehen und beispielsweise neue Biomarker zu identifizieren. Die computergestützte Analyse ermöglicht dabei insbesondere die Untersuchung räumlicher Zusammenhänge im Gewebe sowie deren Beziehung zu klinischen Verläufen.
Neben der stark angewandten, auswertungsorientierten Forschung werden auch methodische Fragen des maschinellen Lernens und der künstlichen Intelligenz in der Domaine der Neuropathologie behandelt.
Als Querschnittsbereich unterstützt die computergestützte Neuropathologie sämtliche Forschungsfelder des Instituts und ermöglicht neue Fragestellungen durch die systematische Nutzung digitaler Daten. Die Arbeiten tragen dazu bei, digitale Pathologie als festen Bestandteil der neuropathologischen Diagnostik und Forschung zu etablieren.
CuBATS - Computer Based Antigen Target Selection
Die CAR T-Zell-Therapie ist eine aufkommende personalisierte Krebsbehandlung. Ihr Erfolg hängt jedoch entscheidend davon ab, geeignete Zielantigene zu identifizieren, die zuverlässig auf Tumorzellen vorkommen und gesundes Gewebe möglichst schonen. Gerade beim Glioblastom ist diese Auswahl aufgrund der hohen Heterogenität äußerst anspruchsvoll.
CuBATS adressiert dieses Problem aus Sicht der computergestützten (Neuro-)Pathology: mittels Immunhistochemie und Bildverarbeitungsalgorithmen werden reproduzierbar und erklärbar Zielantigene für jeden Patienten individuell bestimmt. Dadurch können Expressionsmuster direkt im Gewebekontext analysiert und ihre räumliche Heterogenität sichtbar gemacht werden. Anstatt nur das Vorhandensein eines Markers zu betrachten, erlaubt dieser Ansatz eine Bewertung der tatsächlichen Tumorspezifität im Gewebe — eine zentrale Voraussetzung für sichere CAR-T-Therapien.
CUBATS wird in enger Kooperation mit der Klinik für Neurochirurgie des Universitätsklinikums Würzburg entwickelt. Technisch wird das Projekt durch das Institut DigiHealth der Hochschule Neu Ulm sowie die Universität Würzburg unterstützt.
Krauss S, Spieß E, Hieber D, Schobel J, Kramer F, Müller D. Overcoming Domain Shift in Atypical Mitotic Figure Detection with Deep Ensemble Learning.Studies in Health Technology and Informatics, 336 (2026). doi: 10.3233/SHTI260112.
Bücheler V, Hieber D, Karthan M, Jungbäck N, Dinser M, Pohl C, Pryss R, Liesche-Starnecker F, Schobel J. Eye-Tracking in Digital Pathology: A Vendor-Agnostic Platform for Standardized and Reproducible Eye-Tracking Studies, IEEE 38th International Symposium on Computer-Based Medical Systems (CBMS) (2025), doi: 10.1109/CBMS65348.2025.00190.
Hieber D, Haisch N, Grambow G, Holl F, Liesche-Starnecker F, Pryss R, Schlegel J, Schobel J. Comparing nnU-Net and deepflash2 for Histopathological Tumor Segmentation. Stud Health Technol Inform. 316 (2024). doi: 10.3233/SHTI240487. PMID: 39176815.

Translationale Neuroonkologie: Tumorheterogenität & Microenvironment
Im Bereich der translationalen Neuroonkologie liegt ein zentraler Forschungsschwerpunkt am Institut für Neuropathologie auf der intratumoralen Heterogenität des Glioblastoms, die als wesentliche Grundlage für Therapieresistenz und schnelle Tumorprogression dieser Erkrankung gilt.
Unsere Arbeiten zielen darauf ab, die räumliche und zelluläre Vielfalt innerhalb von Tumoren systematisch zu charakterisieren und mit klinischen Verläufen zu verknüpfen. Durch die Kombination klassischer neuropathologischer Verfahren mit modernen molekularen und digitalen Analyseansätzen untersuchen wir, wie unterschiedliche Tumorzellpopulationen, Microenvironment-Komponenten und immunologische Signaturen zur Dynamik und Adaptation von Glioblastomen beitragen.
Ein weiterer translationaler Schwerpunkt ist die Entwicklung innovativer diagnostischer Strategien zur besseren Tumorcharakterisierung und Therapieüberwachung. Hierzu zählen insbesondere Liquid-Biopsy-Ansätze auf Basis von Liquorproben, an denen wir z.B. Cytokinsignaturen nach intraoperativer Bestrahlung von Hirnmetastasen nachgewiesen haben.
Diese Ansätze tragen dazu bei, die komplexe Biologie maligner Hirntumoren in diagnostisch verwertbare Parameter zu übersetzen und neue Wege für eine personalisierte Therapieüberwachung und Behandlung zu eröffnen.
ORIGIN – Glioblastom-Heterogenität und Therapieresistenz
Ein zentraler Forschungsschwerpunkt unseres Instituts ist die Frage, warum das Glioblastom trotz intensiver Therapie so häufig wiederkehrt. Ein wesentlicher Treiber ist die ausgeprägte intratumorale Heterogenität: Verschiedene Tumorregionen unterscheiden sich morphologisch, epigenetisch und in ihrer Therapieempfindlichkeit, was die Entstehung von Resistenzen begünstigt.
Im Projekt ORIGIN (Overcoming therapy resistance caused by intratumor heterogeneity in glioblastoma by utilizing spatially obtained organoids) entwickeln wir eine innovative translational ausgerichtete Plattform, bei der aus mehreren räumlich getrennten Tumorarealen eines Glioblastoms patientenindividuelle Organoid-Modelle erzeugt werden. Diese ermöglichen es, regionale Unterschiede im Tumor systematisch zu erfassen und ex vivo auf ihre Sensitivität gegenüber Standardtherapien wie Temozolomid sowie neuen zielgerichteten Substanzen zu testen.
Das Projekt erfolgt in enger Zusammenarbeit mit der Würzburger Neurochirurgin Dr. med. Vera Nickl, dessen Arbeitsgruppe über umfassende Expertise in der Etablierung und automatisierten Generierung patientenabgeleiteter Glioblastom-Organoide verfügt. Unser Ziel ist es, Heterogenität nicht nur zu beschreiben, sondern als Grundlage für individualisierte Therapieansätze zu nutzen und neue Strategien zur Überwindung von Therapieresistenz zu entwickeln.
Shiban E, Krauss P, Schaller T, Konietzko I, Mögele T, Jungbäck N, Mielke D, Märkl B, Kahl KH, Mielewczyk Z, Liesche-Starnecker F. A prospective observational study of inflammatory mediators in cerebrospinal fluid after intraoperative radiotherapy of brain tumors. Ther Adv Med Oncol. 17 (2025). doi: 10.1177/17588359251389740. PMID: 41262211. PMCID: PMC12623645.
Wagner A, Brielmaier MC, Kampf C, Baumgart L, Aftahy AK, Meyer HS, Kehl V, Höhne J, Schebesch KM, Schmidt NO, Zoubaa S, Riemenschneider MJ, Ratliff M, Enders F, von Deimling A, Liesche-Starnecker F, Delbridge C, Schlegel J, Meyer B, Gempt J. Fluorescein-stained confocal laser endomicroscopy versus conventional frozen section for intraoperative histopathological assessment of intracranial tumors. Neuro Oncol. 26, 5 (2024). doi: 10.1093/neuonc/noae006. PMID: 38243410. PMCID: PMC11066924.
Godbole S, Voß H, Gocke A, Schlumbohm S, Schumann Y, Peng B, Mynarek M, Rutkowski S, Dottermusch M, Dorostkar MM, Korshunov A, Mair T, Pfister SM, Kwiatkowski M, Hotze M, Neumann P, Hartmann C, Weis J, Liesche-Starnecker F, Guan Y, Moritz M, Siebels B, Struve N, Schlüter H, Schüller U, Krisp C, Neumann JE. Multiomic profiling of medulloblastoma reveals subtype-specific targetable alterations at the proteome and N-glycan level. Nat Commun. 15, 6237 (2024). doi: 10.1038/s41467-024-50554-z. PMID: 39043693. PMCID: PMC11266559.
Prokop G, Wiestler B, Hieber D, Withake F, Mayer K, Gempt J, Delbridge C, Schmidt-Graf F, Pfarr N, Märkl B, Schlegel J, Liesche-Starnecker F. Multiscale quantification of morphological heterogeneity with creation of a predictor of longer survival in glioblastoma. Int J Cancer. 153, 9 (2023). doi: 10.1002/ijc.34665. PMID: 37501565.
Publikationen
Krauss S, Spieß E, Hieber D, Schobel J, Kramer F, Müller D. Overcoming Domain Shift in Atypical Mitotic Figure Detection with Deep Ensemble Learning.Studies in Health Technology and Informatics, 336 (2026). doi: 10.3233/SHTI260112.
Jungbäck N, Grochowski P, Hieber D, Dinser M, Mielewczyk Z, Pfefferkorn T, Muntau B, Richter T, Rieder G, Bayas A, Hirschbühl K, Märkl B, Adam P, Tappe D, Liesche-Starnecker F. Multimodal profiling of immune responses reveals innate-adaptive immune imbalance in human bornavirus encephalitis. Acta Neuropathol Commun 14, 109 (2026). doi: 10.1186/s40478-026-02319-6.
Michelakaki E, Schade B, Boehm B, Kappe E, Suchowski M, Kupca A, Schumacher M, Gager AM, Liesche-Starnecker F, Fiedler S, Schwarz E, Bago Z, Blutke A, Beer M, Rubbenstroth D, Matiasek K. Borna disease virus 1 as cause of fatal meningoencephalomyelitis in wild hedgehogs, Germany, 2022–2025. Emerg Infect Dis (2026). doi: 10.3201/eid3205.250952.
Liesche-Starnecker F, Mielewczyk Z, Grochowski P, Jungbäck N, Adam P, Märkl B, Schlegel J. Hirnsektion in der Allgemeinpathologie. Pathologie (2026).doi: 10.1007/s00292-026-01543-0.
Reitsam NG, Gäble A, Siebenhüter L, Schaller T, Liesche-Starnecker F, Sipos E, Dintner S, Walz C, Babic J, Trepel M, Kircher M, Fincke VE, Johann PD, Märkl B, Lapa C, Enke JS. FAP expression as a marker of malignant transformation enabling in vivo characterization in peripheral nerve sheath tumors: a multimodal and translational study. Acta Neuropathol 151, 11 (2026). doi: 10.1007/s00401-026-02979-7. PMID: 41591566. PMCID: PMC12847211.
Hier finden Sie eine Auswahl an Publikationen vor der Institutsgrüdung. Weitere Publikationen entnehmen Sie bitte den Detailseiten der Ansprechpartner der einzelnen Forschungsschwerpunkte.
Shiban E, Krauss P, Schaller T, Konietzko I, Mögele T, Jungbäck N, Mielke D, Märkl B, Kahl KH, Mielewczyk Z, Liesche-Starnecker F. A prospective observational study of inflammatory mediators in cerebrospinal fluid after intraoperative radiotherapy of brain tumors. Ther Adv Med Oncol. 17 (2025). doi: 10.1177/17588359251389740. PMID: 41262211. PMCID: PMC12623645.
Bücheler V, Hieber D, Karthan M, Jungbäck N, Dinser M, Pohl C, Pryss R, Liesche-Starnecker F, Schobel J. Eye-Tracking in Digital Pathology: A Vendor-Agnostic Platform for Standardized and Reproducible Eye-Tracking Studies, IEEE 38th International Symposium on Computer-Based Medical Systems (CBMS) (2025), doi: 10.1109/CBMS65348.2025.00190.
Vollmuth Y, Jungbäck N, Grochowski P, Mögele T, Stark L, Zarrabi NS, Schlegel J, Schaller T, Märkl B, Matiasek K, Liesche-Starnecker F. Mapping Bornavirus encephalitis-A comparative study of viral spread and immune response in human and animal dead-end hosts. PLoS Pathog 21, 8 (2025). doi: 10.1371/journal.ppat.1013400. PMID: 40758738. PMCID: PMC12338802.
Jungbäck N, Vollmuth Y, Mögele T, Grochowski P, Schlegel J, Schaller T, Märkl B, Herden C, Matiasek K, Tappe D, Liesche-Starnecker F. Neuropathology, pathomechanism, and transmission in zoonotic Borna disease virus 1 infection: a systematic review. Lancet Infect Dis. 25, 4 (2025). doi: 10.1016/S1473-3099(24)00675-3. PMID: 39793593.
Wagner A, Brielmaier MC, Kampf C, Baumgart L, Aftahy AK, Meyer HS, Kehl V, Höhne J, Schebesch KM, Schmidt NO, Zoubaa S, Riemenschneider MJ, Ratliff M, Enders F, von Deimling A, Liesche-Starnecker F, Delbridge C, Schlegel J, Meyer B, Gempt J. Fluorescein-stained confocal laser endomicroscopy versus conventional frozen section for intraoperative histopathological assessment of intracranial tumors. Neuro Oncol. 26, 5 (2024). doi: 10.1093/neuonc/noae006. PMID: 38243410. PMCID: PMC11066924.
Godbole S, Voß H, Gocke A, Schlumbohm S, Schumann Y, Peng B, Mynarek M, Rutkowski S, Dottermusch M, Dorostkar MM, Korshunov A, Mair T, Pfister SM, Kwiatkowski M, Hotze M, Neumann P, Hartmann C, Weis J, Liesche-Starnecker F, Guan Y, Moritz M, Siebels B, Struve N, Schlüter H, Schüller U, Krisp C, Neumann JE. Multiomic profiling of medulloblastoma reveals subtype-specific targetable alterations at the proteome and N-glycan level. Nat Commun. 15, 6237 (2024). doi: 10.1038/s41467-024-50554-z. PMID: 39043693. PMCID: PMC11266559.
Ebinger A, Santos PD, Pfaff F, Dürrwald R, Kolodziejek J, Schlottau K, Ruf V, Liesche-Starnecker F, Ensser A, Korn K, Ulrich R, Fürstenau J, Matiasek K, Hansmann F, Seuberlich T, Nobach D, Müller M, Neubauer-Juric A, Suchowski M, Bauswein M, Niller HH, Schmidt B, Tappe D, Cadar D, Homeier-Bachmann T, Haring VC, Pörtner K, Frank C, Mundhenk L, Hoffmann B, Herms J, Baumgärtner W, Nowotny N, Schlegel J, Ulrich RG, Beer M, Rubbenstroth D. Lethal Borna disease virus 1 infections of humans and animals - in-depth molecular epidemiology and phylogeography. Nat Commun. 15, 7908 (2024). doi: 10.1038/s41467-024-52192-x. PMID: 39256401. PMCID: PMC11387626.
Bayas A, Menacher M, Lapa C, Tappe D, Maurer C, Liesche-Starnecker F, Schneider H, Naumann M. 18fluorodeoxyglucose PET/CT as possible early diagnostic tool preceding MRI changes in Borna disease virus 1 encephalitis. Lancet. 403, 10427 (2024). doi: 10.1016/S0140-6736(24)00049-7. PMID: 38368015.
Hieber D, Haisch N, Grambow G, Holl F, Liesche-Starnecker F, Pryss R, Schlegel J, Schobel J. Comparing nnU-Net and deepflash2 for Histopathological Tumor Segmentation. Stud Health Technol Inform. 316 (2024). doi: 10.3233/SHTI240487. PMID: 39176815.
Vollmuth Y, Jungbäck N, Mögele T, Schmidt-Graf F, Wunderlich S, Schimmel M, Rothe C, Stark L, Schlegel J, Rieder G, Richter T, Schaller T, Tappe D, Märkl B, Matiasek K, Liesche-Starnecker F. Comparative study of virus and lymphocyte distribution with clinical data suggests early high dose immunosuppression as potential key factor for the therapy of patients with BoDV-1 infection. Emerg Microbes & Infections 13 (2024). doi: 10.1080/22221751.2024.2350168; PMID: 38687703. PMCID: PMC11107860.
Prokop G, Wiestler B, Hieber D, Withake F, Mayer K, Gempt J, Delbridge C, Schmidt-Graf F, Pfarr N, Märkl B, Schlegel J, Liesche-Starnecker F. Multiscale quantification of morphological heterogeneity with creation of a predictor of longer survival in glioblastoma. Int J Cancer. 153, 9 (2023). doi: 10.1002/ijc.34665. PMID: 37501565.
Liesche-Starnecker F, Schifferer M, Schlegel J, Vollmuth Y, Rubbenstroth D, Delbridge C, Gempt J, Lorenzl S, Schnurbus L, Misgeld T, Rosati M, Beer M, Matiasek K, Wunderlich S, Finck T. Hemorrhagic lesion with detection of infected endothelial cells in human bornavirus encephalitis. Acta Neuropathol. 144, 2 (2022). doi: 10.1007/s00401-022-02442-3. PMID: 35657496. PMCID: PMC9164175.




