Sektion Gynäkologische Onkologie
Grundlagen orientierte und translationale Forschung
Prof. Dr. Lisa Wiesmüller und ihr Team sind auf dem Gebiet der DNA-Reparatur-, Rekombination und Replikation und deren Störungen bei Karzinogenese, Tumorprogression und Alterung international anerkannt. Das Team generierte wertvolle Werkzeuge für Grundlagen orientierte und translationale Forschung und nutzt diese zur Aufklärung molekularer Mechanismen, zur Entwicklung diagnostischer Markersysteme durch Kombination aus funktionellem Testen und Genotypisierung und für die Identifizierung von Zielstrukturen und pharmakologischen Substanzen zum Schutz von Stammzellen vor Therapie-induzierten Leukämien.
Gefördert werden unsere Projekte, an denen auch Forscher aus Argentinien, USA, Finnland, Italien, Israel sowie anderer deutscher Universitäten teilnehmen, unter anderem von der Deutschen Forschungsgemeinschaft (DFG), der Deutschen Krebshilfe, dem Bundesministerium für Bildung und Forschung (BMBF) und der German-Israeli Foundation for Scientific Research and Development (GIF).
Sektionsleitung
Forschungsschwerpunkte
- DNA-Reparatur, DNA-Rekombination und DNA-Replikation
- Altersforschung
- Erbliche Immundefizienz
- Hereditäres Tumorrisiko, Tumorprävention und gezielte Tumortherapie
Forschungsthemen
Bestimmte Formen des Brust- oder Eierstockkrebses werden heute mit sogenannten PARP-Hemmern behandelt. Diese blockieren das Enzym Poly ADP Ribose Polymerase, das bei der Reparatur von DNA-Schäden eine Schlüsselrolle spielt. In unserem Forschungslabor haben wir nun einen Mechanismus entdeckt, der erklären könnte, warum sich bestimmte Krebszellen trotz PARP-Hemmer weiter ungehindert vermehren, also Therapieresistenzen auftreten.
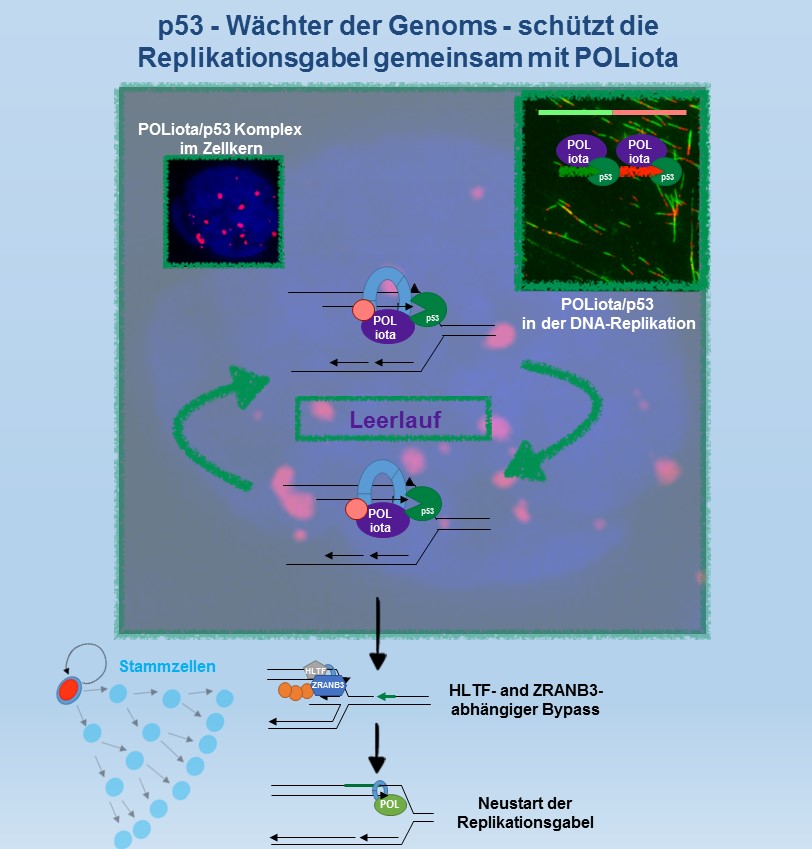
So fanden wir heraus, dass ein bisher unbekannter Schadenstoleranzmechanismus dafür sorgt, Replikationsbarrieren – wie sie beispielsweise durch die pharmakologische Hemmung von PARP entstehen – zu überwinden. Hierbei wird der DNA-Schaden mit Hilfe einer Kopie überbrückt, bei der das Schwesterchromatid als Matrize dient. Der resultierende Bypass ist fehlerfrei und sorgt dafür, dass die DNA-Replikation fortgesetzt wird und sich bestimmte Zellen, darunter leider auch Krebszellen weiter vermehren können. Erstaunlicherweise ist daran das p53-Protein beteiligt, das bisher für seine Wirkung als Tumorsuppressor und „Wächter des Genoms“ bekannt war, da p53 bei DNA-Schäden die Zellteilung stoppt oder sogar Apoptose einleitet, also als „Killer“ wirkt. Bildet p53 jedoch einen Proteinkomplex mit der DNA-Reparatur-Polymerase iota, wirkt es wachstumsfördernd. Dieser Komplex löst einen Leerlaufprozess der DNA-Replikation aus. Dadurch gewinnt die Zelle Zeit bis die Blockade an der Replikationsgabel mit Hilfe strukturspezifischer Enzyme aufgelöst und überbrückt werden kann. Dieser Mechanismus sorgt dafür, dass sich auch Zellen, wo die Replikation gestoppt wird, weiter vermehren können. p53 entfaltet so eine fatale „Heiler“-Wirkung in Krebszellen.
Die Forscher und Ärzte des Teams hoffen, dass sich diese Wirkung von p53 langfristig kontrollieren lässt, sodass noch mehr Krebspatientinnen von der relativ nebenwirkungsarmen PARP-Inhibitor-Therapie profitieren können.
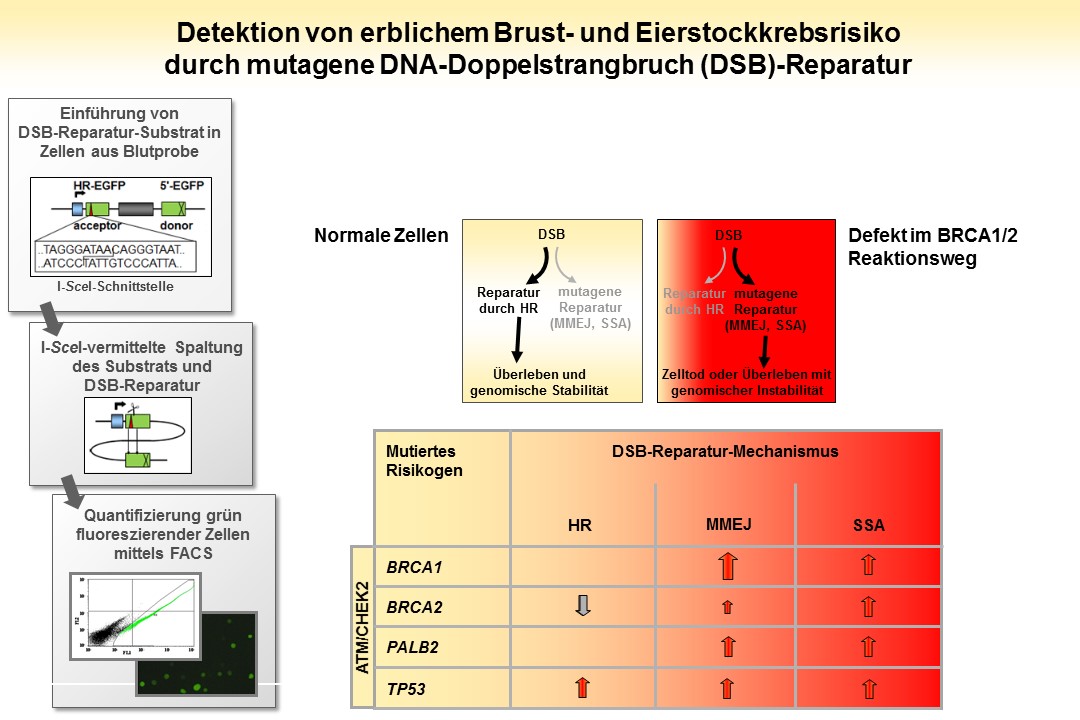
Als außerordentlich vielversprechender Ansatz für weiterführende Applikationen erwies sich das in unserem Labor entwickelte Testsystem für quantitativen und qualitativen Nachweis von DSB-Reparatur-Aktivitäten, basierend auf Detektion von zellulären Fluoreszenz-Signalen (EP1399576). Eine zentrale Anwendung nutzt die Tatsache, dass mutagene DSB-Reparatur mit erblichem Brust- und Eierstockkrebsrisiko wie genetischen Änderungen im BRCA1/2-Weg einhergeht.
In vorangegangenen Arbeiten applizierten wir den Test auf immortalisierte Lymphozyten von Individuen mit Mutationen in unterschiedlichen Risikogenen. Für die Abschätzung der Funktionalität erwies sich die Möglichkeit des Tests zur Unterscheidung zwischen den verschiedenen DSB-Reparatur-Wegen mit Beurteilung der Reparatur-Genauigkeit als bedeutsam (fehlerfrei: Homologe Rekombination, HR; mutagen: microhomology-mediated end joining, MMEJ, und single-strand annealing, SSA). Parallel dazu evaluierten wir den diagnostischen Wert des Testsystems als Indikator für hereditäres Risiko in Lymphozyten aus Blutproben von erkrankten, prädisponierten und gesunden Individuen in Fall-Kontrollstudien und/oder für therapeutisch relevante Tumoreigenschaften an Zellen aus Explantaten.
Die Detektion von mutagener DSB-Reparatur erwies sich gegenüber anderen funktionellen Tests wie der sogenannten Foci-Analyse als überlegen. Der Fluoreszenz basierte Test hat somit hohes Anwendungspotenzial als diagnostisches Marker-System zur Detektion von erhöhtem Brust- und Eierstockkrebsrisiko, auch im Falle des Zusammenspiels mehrerer genetischer Faktoren. Die Herausforderung der nächsten Jahre wird darin bestehen, diese funktionelle Nachweismethode mit neuen Therapien zu kombinieren, welche z. B. unter Einsatz von PARP-Inhibitoren gezielt DSB-Reparatur defiziente Tumore angreifen, um das Ansprechen vorhersagen zu können.
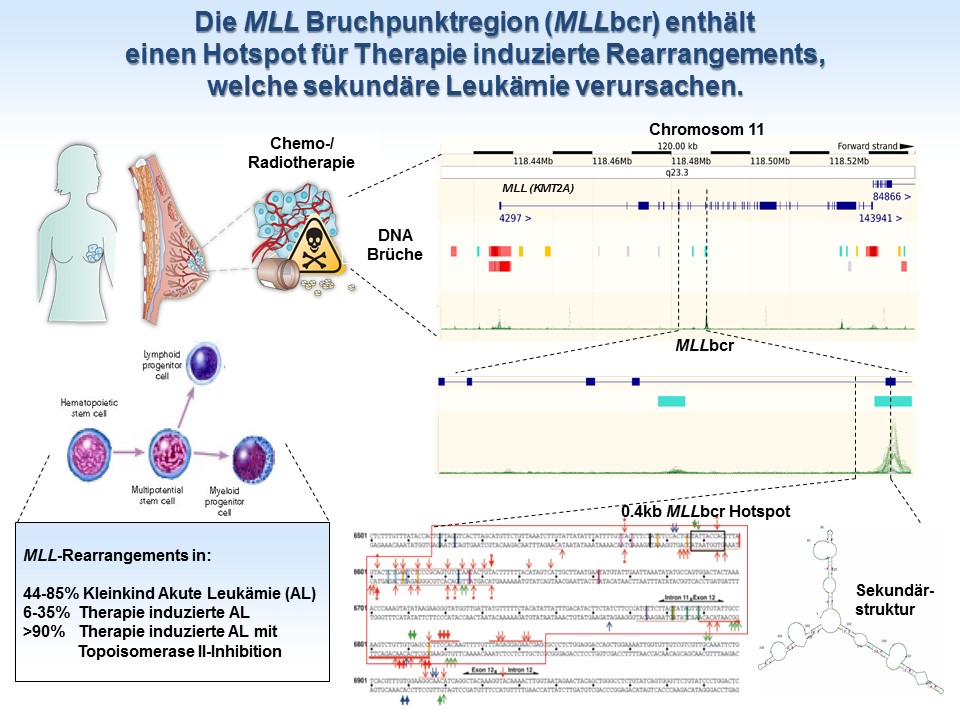
Therapie induzierte, sekundäre Akute Leukämien (tAL) zählen zu den schlimmsten Nebenwirkungen, unter denen ein Krebspatient nach Behandlung der Primärerkrankung durch Chemo- oder Strahlentherapie leiden kann. tAL werden zu 6-35% durch Rearrangements innerhalb der Bruchpunktregion im MLL-Gen (MLLbcr) auf Chromosom 11q23 verursacht und zeichnen sich durch schlechte Prognose aus.
In unserem Team wurde ein zugrunde liegender Mechanismus aufgeklärt, wobei Replikationsstress, also Stolpern der Replikationsmaschinerie an Läsionen, in der MLLbcr als Auslöser für Rearrangements nach Krebstherapien erkannt wurde. Nachgeordnet spaltet Endonuklease G die MLLbcr. Wie beim Antikörper-Klassenwechsel kooperiert Endonuklease G auch hier mit dem Enzym Aktivierungs induzierte Cytidin Deaminase (AID), welches Basenexzisionsreparatur initiiert und damit Brüche generiert. Replikationsstress wird in hämatopoetischen Stammzellen, den Ursprungszellen der Leukämie, nicht nur nach Krebstherapie sondern auch nach Transplantation oder Alterung beobachtet, was die Bedeutung dieses Mechanismus auf Bereiche jenseits der Onkologie ausdehnt.
Folgeprojekte zielen darauf, Krebstherapeutika in Bezug auf das tAL-Risiko einzustufen und präventive pharmakologische Strategien zu entwickeln. Hierfür stehen im Labor entwickelte experimentelle Modellsysteme zur Verfügung, welche MLLbcr-Rearrangements nachahmen. Diese erlauben Substanzbanken systematisch nach Agentien zu durchsuchen (Screenen) und somit Kandidaten zur Reduktion des sekundären Leukämierisikos zu identifizieren. Es konnte bereits ein erster Beweis für dieses Konzept erbracht werden, indem für einen Inhibitor der Basenexzisionsreparatur Unterdrückung der Bruchbildung in der MLLbcr demonstriert wurden. Die gewonnenen Informationen sollen einen Beitrag zur Entwicklung individualisierter Chemotherapie-Protokolle leisten.
Publikationen
Unsere aktuelle Publikationsliste finden Sie unter folgendem Link auf der Internetseite der medizinischen Publikationsdatenbank PubMed.